- Über Uns
- Blog
- Unfruchtbarkeit
- IVF-Behandlungen
- Neue IVF-Fortschritte
- IVF-Behandlung in Zypern
- IVF für Frauen über 40
- IVF für Frauen über 50
- IUI
- Mini-IVF
- IVF + ICSI
- Zytoplasmatische IVF
- Tandem-IVF-Zyklus
- Eizellspende
- Embryonenspende
- Samenspende
- Geschlecht – Geschlechtsauswahl
- Schwangerschafts-Leihmutterschaft
- Gleichgeschlechtliche Leihmutterschaft für Schwule
- Chirurgische Spermienentnahme
- Genetische Diagnostik vor der Implantation, PID
- Einfrieren von Eiern
- Geschlechtsauswahl mithilfe von Spendereizellen
- Prävention von Sichelzellanämie
- FAQ
- Reisen
- Über Uns
- Blog
- Unfruchtbarkeit
- IVF-Behandlungen
- Neue IVF-Fortschritte
- IVF-Behandlung in Zypern
- IVF für Frauen über 40
- IVF für Frauen über 50
- IUI
- Mini-IVF
- IVF + ICSI
- Zytoplasmatische IVF
- Tandem-IVF-Zyklus
- Eizellspende
- Embryonenspende
- Samenspende
- Geschlecht – Geschlechtsauswahl
- Schwangerschafts-Leihmutterschaft
- Gleichgeschlechtliche Leihmutterschaft für Schwule
- Chirurgische Spermienentnahme
- Genetische Diagnostik vor der Implantation, PID
- Einfrieren von Eiern
- Geschlechtsauswahl mithilfe von Spendereizellen
- Prävention von Sichelzellanämie
- FAQ
- Reisen
Stammzelltherapie bei Azoospermie
Behandlung von Azoospermie
Wie kann eine Stammzellbehandlung bei männlicher Unfruchtbarkeit helfen?
Azoospermie ist ein Zustand, bei dem das Ejakulat eines Mannes keine lebenden oder reifen Spermien enthält. In den meisten Fällen kann das Ejakulat Sperma und andere Zellen enthalten, daher ist die Existenz eines flüssigen Ejakulats kein Hinweis auf die Existenz von Spermien. Azoospermie kann in zwei Hauptkategorien unterteilt werden:
Obstruktive Azoospermie: Bei einer Obstruktion können keine Spermien ins Ejakulat abgegeben werden, obwohl die Spermienproduktion aktiv bleibt. Obstruktive Azoospermie kann verschiedene Ursachen haben. Die häufigste Ursache ist heute eine Vasektomie, eine Erkrankung, die den Patienten normalerweise bekannt ist. Es gibt jedoch auch andere Faktoren, die verhindern können, dass Spermien ins Ejakulat gelangen. Zu diesen Faktoren gehören:
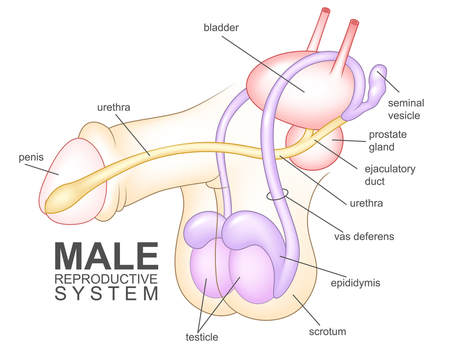
1. Anomalien des Gangsystems
Spermien müssen durch das Gangsystem wandern, um die Harnröhre zu erreichen. Nachdem sie in den Hoden produziert wurden, passieren die Spermien mehrere Strukturen, darunter den Nebenhoden, den Samenleiter (oder Ductus deferens), den Ejakulationsgang und die Harnröhre. Jede Störung des Transports der Spermien durch oder zwischen diesen Strukturen kann ihren Weg behindern. (Eine visuelle Darstellung dieser Strukturen finden Sie in der Abbildung unten.)
2. Ejakulationsstörung
Der Ejakulationsvorgang, bei dem das Sperma vor der Ejakulation in die Harnröhre abgegeben wird, kann gestört sein. Diese Störung kann durch neurologische Schäden oder in einigen Fällen durch unbehandelten Diabetes verursacht werden.
Bei obstruktiver Azoospermie mit chirurgische Techniken zur Spermienextraktion helfen oft dabei, eine akzeptable Anzahl lebensfähiger Spermienzellen für den Einsatz während eines IVF-Zyklus zu erhalten.
Nicht-obstruktive Azoospermie-Behandlung: Nicht-obstruktive Azoospermie (NOA) ist eine Erkrankung, die durch das Fehlen von Spermien im Ejakulat aufgrund einer beeinträchtigten Spermienproduktion in den Hoden gekennzeichnet ist. Im Gegensatz zur obstruktiven Azoospermie, die durch Blockaden im Fortpflanzungstrakt entsteht, entsteht NOA durch eine intrinsische Hodenfunktionsstörung. Dies kann aufgrund genetischer Anomalien (wie Klinefelter-Syndrom oder Mikrodeletionen des Y-Chromosoms), hormoneller Ungleichgewichte oder Schäden an den Hoden durch Infektionen, Traumata, Chemotherapie oder Bestrahlung auftreten. In vielen Fällen bleibt die zugrunde liegende Ursache idiopathisch. NOA ist eine bedeutende Ursache für männliche Unfruchtbarkeit und äußert sich häufig in einem geringeren Hodenvolumen und erhöhten Spiegeln des follikelstimulierenden Hormons (FSH), da der Körper versucht, die verringerte Spermatogenese zu kompensieren. Die Diagnose umfasst in der Regel eine Hormonprofilierung, genetische Tests und gelegentlich eine Hodenbiopsie, um das Fehlen reifer Spermien zu bestätigen.
Der Zweck einer Hodenbiopsie besteht darin, das Hodengewebe gründlich auf das Vorhandensein von weniger reifen Spermien zu untersuchen. Selbst wenn die Spermatogenese (der Prozess der Spermienproduktion und -reifung) nicht vollständig abgeschlossen ist, können frühere Stadien von Spermien vorhanden sein, die möglicherweise verwendet werden können. Das folgende Diagramm zeigt den vollständigen Zyklus der Spermatogenese von Stammzellen bis zu reifen Spermien:
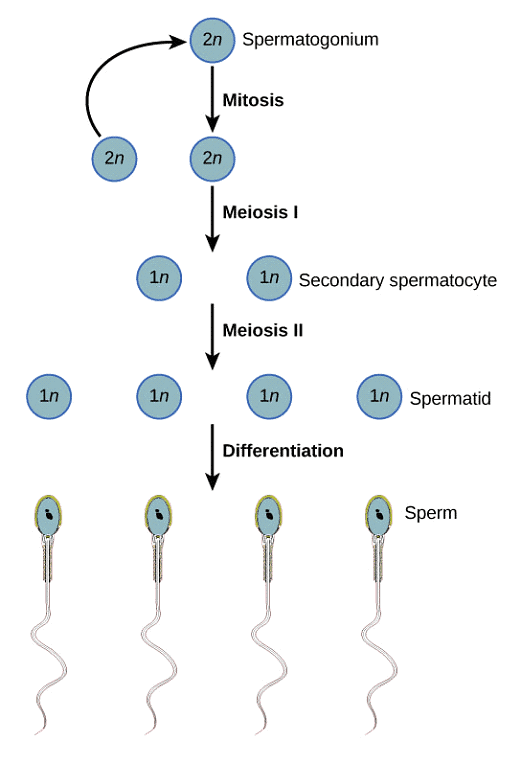
Wenn die Biopsie des Patienten das Vorhandensein von Spermatiden im Spätstadium (verlängerte Spermatiden) zeigt, können späte Spermatiden oft erfolgreich während eines IVF-Zyklus mithilfe von ICSI eingesetzt werden, auch wenn eine natürliche Empfängnis nicht möglich ist. Allerdings führt jedes Stadium der Spermienreifung vor der Bildung verlängerter Spermatiden nicht zu einem erfolgreichen IVF-Ergebnis.
Wenn zu diesem Zeitpunkt keine Keimzellen vorhanden sind und die Diagnose „Sertoli-Zell-Only-Syndrom“ gestellt wird, besteht die einzige andere Möglichkeit, ein Kind zu zeugen, in der Verwendung von Spendersamen oder einer Adoption. Keimzellen sind unreife Samenzellen, die das Potenzial haben, zu wachsen und sich zu reifen Samenzellen zu differenzieren. Diese können als unreife und undifferenzierte Samenzellen betrachtet werden. Dazu gehören:
– Spermatogonie
– Primäre Spermatozyten
– Sekundäre Spermatozyten
– Spermatiden im Frühstadium
– Spermatiden im Spätstadium
Das Vorhandensein von Keimzellen im Hodengewebe ist eine Voraussetzung für die Stammzellentherapie. Der Grund ist einfach. Für die Stammzellenbehandlung verwenden wir mesenchymale Stammzellen aus dem eigenen Fettgewebe des Patienten. Mesenchymale Stammzellen haben ein begrenztes Differenzierungspotenzial. Unter den richtigen Bedingungen können sie sich jedoch in viele Zelltypen differenzieren. Mesenchymale Stammzellen neigen hauptsächlich dazu, sich in umgebende Zelltypen zu differenzieren, es sei denn, sie werden speziell darauf programmiert, sich in einen bestimmten Zelltyp zu differenzieren. Bei unseren Behandlungen findet keine Zellprogrammierung statt. Die aus dem eigenen Fettgewebe des Patienten gewonnenen Stammzellen werden isoliert und in das Hodengewebe injiziert, in dem sich Keimzellen befinden. Da sich Keimzellen in der Umgebung befinden, folgen die Stammzellen ihnen als Vorlage und differenzieren sich ebenfalls in Keimzellen. Dies ist jedoch nur ein Teil des Prozesses. Da vorhandene Keimzellen in den Hoden des Patienten die Spermatogenese nicht abschließen und sich nicht zu voll ausgereiften Spermien entwickeln können, sind zusätzliche Schritte erforderlich, um eine solche Differenzierung zu fördern.
Wenn wir Stammzellen in die Samenkanälchen einführen, injizieren wir auch das plättchenreiche Plasma des Patienten, das aus seiner peripheren Blutprobe gewonnen wird. Plättchenreiches Plasma ist reich an Wachstumsfaktoren, die Zellwachstum und -entwicklung ermöglichen und die Blutversorgung des Gewebes verbessern. Daher profitieren Stammzellen von einer reichhaltigen Infusion von Wachstumsfaktoren in die Umgebung, um ihre Entwicklung zu erleichtern. Darüber hinaus verwenden wir aus der Plazenta gewonnene Exosomen, um die Zellkommunikation in den Hoden zu verbessern.
Die Stammzellentherapie zielt in ihrer Gesamtheit darauf ab:
1- Erhöhen Sie die Population der Keimzellen im Hodengewebe, indem Sie dem Hodengewebe Stammzellen zuführen.
2- Ermöglichen Sie diesen Keimzellen mit Hilfe von Wachstumsfaktoren zu wachsen und sich zu entwickeln.
3- Verbessern Sie die zelluläre Kommunikation und erleichtern Sie die Reaktion auf hormonelle Stimulation mit Hilfe von Exosomen.
Was ist plättchenreiches Plasma (PRP)? PRP ist ein Konzentrat aus Blutplättchen, das aus dem eigenen Blut einer Person gewonnen und mit Wachstumsfaktoren und bioaktiven Proteinen angereichert wird, die die Heilung und Geweberegeneration fördern. PRP wird häufig in medizinischen und ästhetischen Behandlungen verwendet, um die Reparatur beschädigten Gewebes zu beschleunigen, Entzündungen zu reduzieren und die Zellvermehrung zu stimulieren.
Blutplättchen spielen eine Schlüsselrolle bei der Wundheilung und Gewebereparatur, indem sie Wachstumsfaktoren freisetzen wie:
⦁ Von Blutplättchen abgeleiteter Wachstumsfaktor (PDGF): Stimuliert das Zellwachstum und die Bildung neuer Blutgefäße.
⦁ Transformierender Wachstumsfaktor-Beta (TGF-β): Fördert die Gewebereparatur und reduziert Entzündungen.
⦁ Vaskulärer endothelialer Wachstumsfaktor (VEGF): Fördert die Bildung neuer Blutgefäße.
⦁ Epidermaler Wachstumsfaktor (EGF): Unterstützt die Zellregeneration und Wundheilung.
Wenn PRP in einen Zielbereich injiziert wird, rekrutieren und aktivieren diese Wachstumsfaktoren die natürlichen Heilungsprozesse des Körpers, einschließlich der Aktivierung von Stammzellen und der Kollagensynthese.
Was sind Exosomen?
Exosomen sind winzige Nanovesikel, die sowohl in Zwischenräumen als auch in Körperflüssigkeiten vorkommen. Aufgrund ihrer Größe wurden Exosomen schon immer als Artefakte oder Zellmüll ohne physiologische Funktion angesehen. Dank der Fortschritte in der medizinischen Forschung weiß man heute jedoch, dass sie Teil eines ausgeklügelten intrazellulären Kommunikationssystems sind.
Exosomen sind für ihre Beteiligung an allen Arten der zellulären Kommunikation bekannt. Sie liefern lokale autokrine Signale zwischen ähnlichen Zelltypen, lokale parakrine Signale zwischen verschiedenen Zelltypen sowie entfernte endokrine Signale. Ihre Beteiligung an solch umfangreichen zellulären Signalübertragungen hat ihnen den Namen „Signalosomen“ eingebracht. Wenn Exosomen in den Körper eingeführt werden, verbessern sie die Kommunikation über alle Kanäle, was zur allgemeinen Gesundheit und Funktion der Zellen beiträgt.
Im Vergleich zu adulten Stammzellen enthalten Exosomen 300% mehr Wachstumsfaktoren, die für das Zellwachstum, die Entwicklung und die Regeneration unerlässlich sind. Exosomen können über eine intravenöse Infusion verabreicht oder durch direkte Injektion an eine bestimmte Stelle geleitet werden.
Wie wird die Stammzellentherapie durchgeführt?
Im Nordzypern-IVF-Zentrum verwenden wir für die Behandlung von nicht-obstruktiver Azoospermie Stammzellentherapien mit einem Cocktail aus mesenchymalen Stammzellen, plättchenreichem Plasma und Exosomen. Die Isolierung der Stammzellen erfordert einen chirurgischen Eingriff namens Fettabsaugung.
Der Fettabsaugung zum Erhalten mesenchymale Stammzellen (MSCs) ist eine minimalinvasive chirurgische Technik zur Entnahme von Fettgewebe, das eine reichhaltige Quelle für MSCs ist. Der chirurgische Eingriff umfasst mehrere Schritte:
1. Präoperative Vorbereitung:
Der Patient wird medizinisch untersucht, um sicherzustellen, dass er für den Eingriff geeignet ist. Dazu gehören eine Reihe von Hormontests, möglicherweise eine Untersuchung des Hodensacks und eine Hodenbiopsie zur Beurteilung der Zellularität der Samenkanälchen.
Der Patient wird außerdem gebeten, eine Reihe von Bluttests durchzuführen, um die Leber- und Nierenfunktion sowie bestimmte Tumormarker wie Alpha-Fetoprotein (AFP) und Beta-Human-Choriongonadotropin (b-hCG) zu überprüfen.
2. Injektion einer Tumeszenzlösung:
Eine Tumeszenzlösung, die Kochsalzlösung, Lidocain (ein Lokalanästhetikum) und Adrenalin (zur Verringerung der Blutung) enthält, wird in den Zielbereich injiziert. Diese Lösung hilft, Fettzellen zu lösen, lindert Schmerzen und minimiert Blutungen während des Eingriffs.
3. Fettabsaugung (Liposuktion):
Es wird ein kleiner Einschnitt in die Haut gemacht und ein Kanüle (ein dünner, hohler Schlauch) wird eingeführt. Die Kanüle ist an ein Vakuumgerät angeschlossen, das Fettgewebe vorsichtig aus Bereichen wie Bauch, Oberschenkeln oder Gesäß absaugt.
4. Verarbeitung des Fettgewebes:
Das extrahierte Fett wird in sterilen Behältern gesammelt und verarbeitet, um MSCs zu isolieren. Die Verarbeitung umfasst:
Zentrifugation um Fett von anderen Bestandteilen wie Blut und Körperflüssigkeiten zu trennen,
Enzymatische Verdauung Verwendung von Kollagenase zum Abbau der extrazellulären Matrix und zur Freisetzung von MSCs.
Filtration und Reinigung um die MSCs zu reinigen und Rückstände zu entfernen.
5. Wiedereinpflanzung:
Die MSCs werden mit PRP und Exosomen zu einem Cocktail verarbeitet und direkt in die Zielbereiche der Hoden injiziert. Der gesamte Vorgang wird innerhalb weniger Stunden durchgeführt, während der Patient unter Sedierung steht. Daher werden die Fettabsaugung und die Reimplantation in einem Durchgang durchgeführt, ohne dass zwei separate Sedierungen erforderlich sind.
Obwohl der Eingriff im Allgemeinen sicher ist, können an der Stelle der Fettabsaugung oder der Reimplantation leichte Blutergüsse, Infektionen oder Beschwerden auftreten. Diese Technik wird in der regenerativen Medizin aufgrund der hohen Wirksamkeit und Vielseitigkeit von aus Fettgewebe gewonnenen MSCs häufig eingesetzt.
Erforderliche Aufenthaltsdauer in Zypern:
Die meisten unserer Patienten reisen aus dem Ausland an. Aufgrund von Verpflichtungen bei der Arbeit oder zu Hause kann die Reisezeit begrenzt sein. Aus diesem Grund bitten wir darum, die Voruntersuchungen/Biopsie vor der Ankunft des Patienten vor Ort durchzuführen, damit die Aufenthaltsdauer auf Zypern minimiert werden kann. Für die Stammzellentherapie werden Sie voraussichtlich etwa 3 Tage auf Zypern bleiben. Dies gibt uns genügend Zeit, um die notwendigen präoperativen Tests durchzuführen, Ihre Blutprobe zu entnehmen und den Eingriff durchzuführen. Sie werden voraussichtlich über Nacht zur Beobachtung in unserem Krankenhaus bleiben und können am nächsten Tag wieder nach Hause reisen.
Was ist nach dem Eingriff zu erwarten? Erfolgsraten:
Nach der Injektion von Stammzellen muss man drei Monate warten, bis die Wirkung sichtbar wird. Die Spermatogenese (Produktion und Reifung der Spermien) dauert etwa 65 bis 70 Tage. Daher benötigen implantierte Stammzellen diese Zeitspanne, bevor wir eine Wirkung beobachten können.
Der Erfolg des Verfahrens hängt weitgehend von der Zellularität des Hodengewebes ab. Patienten, die bereits Spermatiden im frühen oder späten Stadium in ihrem Hodengewebe haben (JOhnsen-Score von 7 oder 8) sind die Patientengruppe, die die höchsten Erfolgschancen bei der Stammzellentherapie hat. In den meisten Fällen können wir nach drei Monaten reife Spermien im Ejakulat beobachten. Obwohl die Anzahl der reifen Spermien im Ejakulat für eine natürliche Empfängnis nicht ausreicht, planen und führen wir bei dieser Patientengruppe häufig einen erfolgreichen IVF-Zyklus durch. Die Chance, bei dieser Patientengruppe erfolgreich reife Spermien im Ejakulat zu erhalten, liegt bei etwa 75%.
Patienten, die keine Spermatiden in den Samenkanälchen haben (vielleicht einige), aber sekundäre Spermatozyten (Johnsen-Score von 5 bis 6) erwarten ebenfalls eine Verbesserung ihrer spermatogenen Aktivität, die zu reifen Spermien führen kann, die ins Ejakulat gelangen können. Bei dieser Patientengruppe ist das Vorkommen reifer Spermien im Ejakulat jedoch seltener. Wir gehen bei dieser Patientengruppe davon aus, in einer Hodenbiopsie reifende Spermatiden zu finden, die während eines IVF-Zyklus verwendet werden können. Wenn die drei Monate nach der Stammzellentherapie durchgeführte Spermienanalyse keine Spermien im Ejakulat anzeigt, besteht der nächste Schritt darin, eine testikuläre Spermienextraktion zu organisieren, um lebensfähige Spermien zu erhalten, die während der ICSI verwendet werden können. Die Chance, bei dieser Patientengruppe erfolgreich reife Spermien im Ejakulat zu erhalten, liegt bei etwa 25%. Die Chance, entweder im Ejakulat oder über TESE lebensfähige Spermien zu finden, liegt bei etwa 40%.
Patienten, die nur primäre Spermatozyten in ihren Samenkanälchen haben (Johnsen-Score von 4) sind nach der Stammzellenbehandlung wahrscheinlich keine reifen Spermien im Ejakulat zu beobachten. In den meisten Fällen sehen wir eine Verbesserung der spermatogenen Aktivität in dem Sinne, dass das Gewebe mehr Keimzellen enthält. Bei einer großen Mehrheit der Patienten finden wir jedoch keine ausreichend reifen Spermien, um sie während der ICSI zu verwenden. Der Erfolg bei dieser Patientengruppe kann auf 15% geschätzt werden, d. h. 15% der Patienten werden ausreichend reife Spermien haben, die in einem IVF-Zyklus verwendet werden können.
Basierend auf unseren bisherigen Patientenstatistiken, Patienten mit ausschließlich Spermatogonien in den Samenkanälchen (Johnsen-Score von 3) haben wahrscheinlich eine Chance, nach der Stammzellenbehandlung ausreichend reife Spermien zu haben, die bei einer ICSI verwendet werden können.
Wir erwarten kein erfolgreiches Ergebnis bei der Patientengruppe mit einem Johnsen-Score von 2 oder darunter (nur Sertoli-Zellen-Syndrom oder keine Zellen).
Was ist ein Johnsen-Score?
Der Johnsen-Punktesystem ist eine histologische Methode zur Auswertung von Hodenbiopsieproben durch Bewertung der Spermatogenese (Spermienproduktion) in den Samenkanälchen. Das 1970 von SG Johnsen entwickelte System weist jedem Samenkanälchen einen numerischen Wert zu, der auf dem Vorhandensein und der Reife der Keimzellen sowie dem Gesamtzustand der Spermatogenese basiert. Es wird häufig zur Beurteilung männlicher Unfruchtbarkeit verwendet.
Bewertungskriterien
Jedem Samenkanälchen wird eine Punktzahl zugewiesen, die von 1 bis 10 basierend auf den folgenden Kriterien:
Punktzahl 10: Vollständige Spermatogenese mit vielen sichtbaren Spermien.
Punktzahl 9: Leicht reduzierte Spermatogenese, jedoch mit vielen Spermatiden im Spätstadium.
Punktzahl 8: Wenige späte Spermatiden, was auf eine mäßig beeinträchtigte Spermatogenese hinweist.
Punktzahl 7: Vorhandensein vieler früher Spermatiden, aber keiner späten Spermatiden oder Spermien.
Punktzahl 6: Vorhandensein weniger früher Spermatiden, aber keiner späten Spermatiden oder Spermien.
Punktzahl 5: Viele Spermatozyten vorhanden, aber keine Spermatiden oder Spermien.
Punktzahl 4: Wenige Spermatozyten vorhanden, aber keine Spermatiden oder Spermien.
Punktzahl 3: Spermatogonien (Keimzellvorläufer) vorhanden, jedoch keine Spermatozyten, Spermatiden oder Spermien.
Punktzahl 2: Nur Sertoli-Zellen, keine Keimzellen vorhanden.
Punktzahl 1: In der Biopsie sind keine Samenkanälchen vorhanden (extreme Hodenschädigung).
Interpretation der Ergebnisse
A höhere Punktzahl weist auf eine normale oder nahezu normale Spermatogenese hin.
A niedrigere Punktzahl spiegelt eine beeinträchtigte oder fehlende Spermatogenese wider.
Durch Berechnung der mittlerer Johnsen-Score Anhand aller untersuchten Tubuli können wir den Grad der spermatogenen Beeinträchtigung quantifizieren und fundierte Entscheidungen zu Behandlungsmöglichkeiten treffen, wie z. B. der Fortführung von Techniken der assistierten Reproduktion, der Verwendung von Stammzellenbehandlungen oder der Prüfung von Spenderoptionen.
Kosten einer Stammzelltherapie bei nicht-obstruktiver Azoospermie:
Die Kosten für die Stammzellentherapie zur Behandlung der nicht-obstruktiven Azoospermie betragen 7.000 Euro, inklusive PRP-Protokoll, Fettabsaugung und Stammzellenreinigung, Exosomen und Implantation in das Hodengewebe. Eine Übernachtung im Krankenhaus ist in diesem Angebot ebenfalls enthalten.
Bitte zögern Sie nicht, kontaktiere uns für mehr Informationen.
Neue Fortschritte in der IVF-Technologie
IVF-Zentrum Nordzypern
Das IVF-Zentrum Nordzypern ist eine patientenorientierte Fruchtbarkeitsklinik mit Sitz in „Elite-Forschungs- und Chirurgiekrankenhaus“ in Nikosia, Zypern. Unsere Klinik ist eine der fortschrittlichsten Fruchtbarkeitskliniken der Welt und bietet eine größere Auswahl an Behandlungsmöglichkeiten zu erschwinglichen Preisen.
Kontakt
Telefon
Englisch: +90 548 875 8000
Französisch: +90 548 876 8000
Türkisch: +90 542 869 8000
Arabisch: +90 548 875 8000
Deutsch: +90 548 830 1987
Russisch: +90 548 828 9955
info@northcyprusivf.net
© 2020 LowCostIVF – Alle Rechte vorbehalten. Datenschutz-Bestimmungen


