- О нас
- Блог
- Бесплодие
- ЭКО лечение
- Новые достижения ЭКО
- Митохондриальная заместительная терапия!
- Лечение ЭКО на Кипре
- ВМИ
- Мини ЭКО
- ЭКО + ИКСИ
- Цитоплазматическое ЭКО
- Тандемный цикл ЭКО
- Пожертвование яйцеклеток
- Донорство эмбрионов
- Донорство спермы
- Пол – Выбор пола
- Гестационное суррогатное материнство
- Суррогатное материнство однополых геев
- Хирургическое извлечение спермы
- Преимплантационная генетическая диагностика ПГД
- Заморозка яиц
- Выбор пола с использованием донорских яйцеклеток
- Профилактика серповидноклеточной анемии
- Часто задаваемые вопросы
- Путешествовать
- О нас
- Блог
- Бесплодие
- ЭКО лечение
- Новые достижения ЭКО
- Митохондриальная заместительная терапия!
- Лечение ЭКО на Кипре
- ВМИ
- Мини ЭКО
- ЭКО + ИКСИ
- Цитоплазматическое ЭКО
- Тандемный цикл ЭКО
- Пожертвование яйцеклеток
- Донорство эмбрионов
- Донорство спермы
- Пол – Выбор пола
- Гестационное суррогатное материнство
- Суррогатное материнство однополых геев
- Хирургическое извлечение спермы
- Преимплантационная генетическая диагностика ПГД
- Заморозка яиц
- Выбор пола с использованием донорских яйцеклеток
- Профилактика серповидноклеточной анемии
- Часто задаваемые вопросы
- Путешествовать
Женское бесплодие
Диагностика и управление
Диагностика женского бесплодия часто сложнее, чем диагностика мужского бесплодия. В то время как мужское бесплодие иногда можно оценить с помощью одного анализа спермы, оценка женского бесплодия обычно требует серии обширных тестов и обследований, которые могут дать или не дать окончательный диагноз.
Женщины вносят не только яйцеклетку, но и необходимую среду для развития эмбриона в жизнеспособное человеческое существо. Хотя женское бесплодие обычно связано с проблемами со здоровьем яйцеклеток, различные состояния яичников и матки также могут влиять на способность женщины к естественному зачатию. Существуют установленные руководящие принципы для диагностики первичного женского бесплодия; однако любая оценка бесплодия должна начинаться с тщательного изучения истории болезни. Следующие вопросы могут помочь в диагностике и лечении первичного женского бесплодия:
⦁ Вы когда-нибудь были беременны?
⦁ У вас когда-нибудь был выкидыш? Если да, то на каком сроке беременности произошел выкидыш?
⦁ Есть ли у вас семейная история бесплодия?
⦁ У вас регулярный менструальный цикл?
⦁ Вы недавно проходили обследование на инфекционные заболевания, в том числе венерические?
⦁ У вас есть домашние животные?
Ответы на каждый из этих вопросов могут предоставить важную информацию специалисту по фертильности. Например, наличие домашних животных может повысить вероятность заражения женщин инфекциями, которые могут вызвать бесплодие, такими как токсоплазмоз. Аналогичным образом, семейный анамнез бесплодия может указывать на генетические причины бесплодия. Во время любого обследования на бесплодие пациенты не должны довольствоваться ни чем иным, как всеобъемлющей историей болезни. Копия нашей формы истории болезни находится на нашей странице «Контакты». Хотя анкета — это только начало обследования на бесплодие, эти вопросы могут помочь выявить потенциальные причины бесплодия, но следующим шагом является оценка репродуктивной физиологии как мужчины, так и женщины. В частности, гормональное тестирование может предоставить информацию о функции яичников женщины и помочь в назначении лечения.
Каковы наиболее распространённые причины женского бесплодия?
1- Проблемы с овуляцией
Овуляция является важнейшей частью женского репродуктивного цикла и необходима для зачатия. Во время овуляции зрелая яйцеклетка высвобождается из одного из яичников и становится доступной для оплодотворения спермой. У большинства женщин этот процесс происходит один раз за цикл, как правило, примерно за две недели до начала менструации. Яйцеклетка проходит через фаллопиеву трубу, где она может быть оплодотворена, а затем перемещается в матку для имплантации.
Когда овуляция не происходит регулярно или вообще не происходит, это называется овуляторной дисфункцией. Овуляторная дисфункция является одной из основных причин женского бесплодия, на нее приходится около 25-30% случаев бесплодия. Женщины, испытывающие проблемы с овуляцией, могут иметь нерегулярные менструальные циклы, пропущенные месячные или даже полное отсутствие менструаций (аменорея). Однако у некоторых женщин с овуляторной дисфункцией менструальные циклы могут быть регулярными, что затрудняет выявление основной проблемы без дополнительных тестов.
Типы нарушений овуляции
Проблемы с овуляцией могут проявляться в различных формах, каждая из которых имеет различные основные причины. Наиболее распространенные овуляторные нарушения включают:
1. Ановуляция: Это полное отсутствие овуляции, когда яичники не выпускают яйцеклетку во время менструального цикла. Ановуляция обычно связана с гормональным дисбалансом, синдромом поликистозных яичников (СПКЯ) или первичной недостаточностью яичников (ПНО).
2. Олигоовуляция: В этом случае овуляция происходит нерегулярно или нечасто. Женщины с олигоовуляцией могут иметь непредсказуемые циклы или большие промежутки между менструациями, что может затруднить выбор времени для полового акта для зачатия. Олигоовуляция также часто связана с такими состояниями, как СПКЯ или другими гормональными проблемами.
3. Дефект лютеиновой фазы (ДЛФ): Это состояние возникает, когда лютеиновая фаза — период после овуляции — не производит достаточного количества прогестерона для поддержки оплодотворенной яйцеклетки. Низкий уровень прогестерона может помешать слизистой оболочке матки достаточно утолщаться, что затрудняет имплантацию и развитие эмбриона, что может привести к ранней потере беременности.
Причины проблем с овуляцией
Проблемы с овуляцией в первую очередь коренятся в гормональном дисбалансе и нарушении сигналов между мозгом и репродуктивными органами. Наиболее распространенные причины нарушений овуляции включают:
1. Синдром поликистозных яичников (СПКЯ): СПКЯ является одной из наиболее распространенных причин овуляторной дисфункции, затрагивающей около 5-10% женщин репродуктивного возраста. Женщины с СПКЯ обычно имеют повышенный уровень андрогенов (мужских гормонов), которые мешают овуляции. СПКЯ может привести к ановуляции, нерегулярным менструациям и другим метаболическим проблемам, таким как резистентность к инсулину.
2. Дисфункция гипоталамуса: Гипоталамус в мозге регулирует многие функции организма, включая высвобождение гонадотропин-рилизинг-гормона (ГнРГ), который сигнализирует гипофизу о необходимости вырабатывать гормоны, необходимые для овуляции: фолликулостимулирующий гормон (ФСГ) и лютеинизирующий гормон (ЛГ). Стресс, сильная потеря веса, чрезмерные физические нагрузки или расстройства пищевого поведения могут нарушить функцию гипоталамуса, что приводит к нерегулярной или отсутствующей овуляции.
3. Первичная недостаточность яичников (ПНЯ): Также известная как преждевременная недостаточность яичников, ПНЯ возникает, когда яичники теряют нормальную функцию до 40 лет. Это состояние иногда возникает из-за генетических факторов, аутоиммунных расстройств или определенных медицинских процедур (например, химиотерапии). ПНЯ может привести к снижению выработки эстрогена, нерегулярным циклам и, в конечном итоге, прекращению овуляции.
4. Гиперпролактинемия: Повышенный уровень пролактина, гормона, отвечающего за выработку молока, может подавлять овуляцию, нарушая баланс репродуктивных гормонов. Это состояние может быть вызвано приемом лекарств, опухолями гипофиза или проблемами со щитовидной железой.
5. Заболевания щитовидной железы: Как гипертиреоз (чрезмерная активность щитовидной железы), так и гипотиреоз (недостаточная активность щитовидной железы) могут нарушать нормальные менструальные и овуляторные циклы. Гормоны щитовидной железы играют важную роль в регуляции репродуктивной системы организма, и любой дисбаланс может привести к проблемам с овуляцией.
Симптомы проблем с овуляцией
Симптомы проблем с овуляцией могут сильно различаться в зависимости от конкретного расстройства. Распространенные симптомы, которые могут указывать на овуляторную дисфункцию, включают:
• Нерегулярные менструальные циклы (слишком длинные, слишком короткие или непредсказуемые)
• Отсутствие менструации (аменорея)
• Обильные или очень слабые менструальные кровотечения
• Отсутствие предменструальных симптомов (болезненность груди, вздутие живота)
• Трудность прогнозирования овуляции (нерегулярные колебания базальной температуры тела)
• Угри, избыточное оволосение лица и тела, увеличение веса (особенно у женщин с СПКЯ)
Эти симптомы не подтверждают наличие проблем с овуляцией, но могут быть индикаторами, требующими дальнейшего обследования у медицинского специалиста.
Диагностика проблем с овуляцией
Для диагностики нарушений овуляции может быть проведен ряд обследований и тестов. Они включают:
1. История болезни и физикальное обследование: Тщательный сбор анамнеза и медицинский осмотр могут выявить потенциальные основные причины, такие как факторы образа жизни, изменения веса или уровень стресса, которые могут влиять на овуляцию.
2. Отслеживание овуляции: Женщин могут попросить отслеживать менструальные циклы, базальную температуру тела или использовать наборы для прогнозирования овуляции. Анализы крови на прогестерон, взятые во время лютеиновой фазы, могут подтвердить, произошла ли овуляция.
3. Гормональное тестирование: Анализы крови позволяют оценить уровень основных гормонов, включая ФСГ, ЛГ, эстроген, пролактин, тестостерон и гормоны щитовидной железы, чтобы определить любые дисбалансы, которые могут влиять на овуляцию.
4. УЗИ: Трансвагинальное УЗИ может помочь визуализировать яичники и обнаружить наличие фолликулов, кист или других аномалий. Эта визуализация может быть особенно полезна при диагностике СПКЯ или мониторинге реакции яичников на гормональное лечение, если проводится лечение бесплодия.
5. Дополнительные тесты для выявления основных заболеваний: Если первоначальное тестирование указывает на такую проблему, как синдром яичников с синдромом поликистозных яичников или заболевание щитовидной железы, для подтверждения диагноза могут быть проведены дополнительные тесты.
Проблемы с овуляцией могут усложнить зачатие, поскольку нерегулярная или отсутствующая овуляция снижает количество возможностей для оплодотворения яйцеклетки. Даже когда овуляция происходит, такие состояния, как дефект лютеиновой фазы или некачественные яйцеклетки, могут помешать имплантации или повысить риск выкидыша. К счастью, многие нарушения овуляции поддаются лечению, и достижения в области репродуктивной медицины предлагают различные варианты для женщин, страдающих бесплодием, связанным с овуляцией.
2- Проблемы с фаллопиевыми трубами
Заблокированные или поврежденные фаллопиевы трубы являются существенной причиной женского бесплодия, поскольку они нарушают нормальный путь для встречи яйцеклетки и сперматозоида, тем самым предотвращая оплодотворение. Фаллопиевы трубы, которые соединяют яичники с маткой, играют важную роль в репродуктивном процессе. Каждый месяц после овуляции яйцеклетка высвобождается из одного из яичников и перемещается по фаллопиевой трубе, где она может встретиться со спермой и подвергнуться оплодотворению. После оплодотворения эмбрион продолжает двигаться по трубе, пока не достигнет матки для имплантации. Когда одна или обе фаллопиевы трубы заблокированы или повреждены, это путешествие затруднено, что делает естественное зачатие трудным или невозможным.
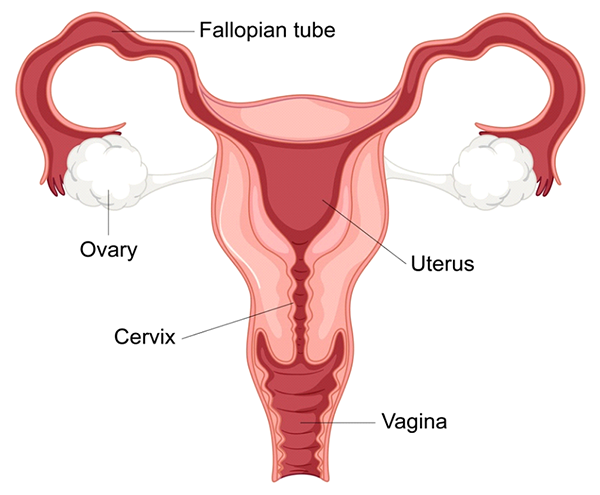
Как повреждение фаллопиевых труб влияет на фертильность
Повреждение или непроходимость маточных труб могут повлиять на фертильность следующими способами:
a) Препятствование сперматозоидам достичь яйцеклетки: если фаллопиевы трубы полностью заблокированы, сперматозоид не может достичь яйцеклетки, и оплодотворение не может произойти. Эта ситуация известна как трубный фактор бесплодия, который составляет около 25-35% случаев женского бесплодия.
б) Препятствование захвату яйцеклетки: повреждение фимбрий (бахромчатых концов фаллопиевых труб около яичников) может помешать захвату яйцеклетки и ее втягиванию в фаллопиеву трубу после овуляции. Без этого процесса яйцеклетка не может спуститься по трубе на встречу со сперматозоидом.
c) Предотвращение транспортировки эмбриона: Если частично заблокированная труба допускает оплодотворение, но препятствует прохождению оплодотворенной яйцеклетки (эмбриона), это может привести к внематочной беременности. Это серьезное состояние, при котором эмбрион имплантируется и растет в фаллопиевой трубе, а не в матке, что может привести к медицинским осложнениям и требует немедленного лечения.
d) Препятствование имплантации в матку: даже если труба только частично заблокирована или повреждена, это может повлиять на своевременную транспортировку эмбриона в матку. Задержка транспортировки эмбриона может снизить вероятность успешной имплантации или увеличить риск имплантации в неподходящем месте.
Причины закупорки или повреждения маточных труб
1. Воспалительные заболевания органов малого таза (ВЗОМТ): ВЗОМТ — это инфекция женских репродуктивных органов, часто вызываемая инфекциями, передающимися половым путем (ИППП), такими как хламидиоз или гонорея. При отсутствии лечения эти инфекции могут привести к воспалению и рубцеванию фаллопиевых труб, вызывая частичную или полную непроходимость. ВЗОМТ — одна из наиболее распространенных причин трубного фактора бесплодия.
2. Эндометриоз: Эндометриоз — это состояние, при котором ткань, похожая на слизистую оболочку матки, разрастается за пределами матки, часто на яичниках, фаллопиевых трубах или тазовой слизистой оболочке. Эндометриальные имплантаты на фаллопиевых трубах или около них могут вызывать спайки, воспаление или рубцевание, что приводит к закупорке или ограничению движения труб.
3. Трубная хирургия: предыдущие операции на фаллопиевых трубах, такие как процедуры по восстановлению трубной беременности, удалению кист или лечению трубных инфекций, могут привести к образованию рубцов и спаек, которые блокируют трубы. Женщины, перенесшие перевязку маточных труб (хирургическую стерилизацию), также могут страдать бесплодием из-за преднамеренной закупорки труб.
4. Спайки после абдоминальной или тазовой хирургии: Операции, затрагивающие брюшную полость или таз, такие как аппендэктомия, кесарево сечение или операции по удалению кист яичников, могут привести к образованию рубцовой ткани вокруг фаллопиевых труб. Эти спайки могут препятствовать проходимости труб или ограничивать их движение, влияя на путь яйцеклетки в матку.
5. Гидросальпинкс: Гидросальпинкс — это состояние, при котором одна или обе фаллопиевы трубы блокируются и заполняются жидкостью. Это состояние часто является результатом инфекций, ВЗОМТ или эндометриоза. Жидкость в гидросальпинксе может быть токсичной для эмбрионов и может снизить вероятность успеха экстракорпорального оплодотворения (ЭКО), если ее не лечить.
6. Врожденные аномалии: в редких случаях некоторые женщины могут родиться со структурными аномалиями фаллопиевых труб, которые могут привести к непроходимости или дисфункции.
Диагностика непроходимости или повреждения маточных труб
Для диагностики непроходимости или повреждения маточных труб часто используются следующие методы диагностики:
1. Гистеросальпингография (ГСГ): HSG — это рентгенологическая процедура, при которой в матку и маточные трубы вводится специальный краситель для оценки их структуры. Краситель виден на рентгеновских снимках и может выявить закупорку или аномалии в трубах.
2. Соногистерография: Эта процедура похожа на HSG, но вместо рентгена используется ультразвук. В матку вводится солевой раствор, что позволяет врачу осмотреть маточные трубы и оценить наличие закупорок или повреждений.
3. Лапароскопия: Лапароскопия — это минимально инвазивная хирургическая процедура, которая заключается в введении небольшой камеры через крошечный разрез в брюшной полости. Эта процедура позволяет врачу напрямую осмотреть маточные трубы, удалить незначительные закупорки или спайки и оценить состояние окружающих органов малого таза. Лапароскопия часто проводится, когда другие диагностические тесты не дали окончательных результатов или когда присутствуют симптомы эндометриоза или тазовых спаек.
4. Тест на антитела к хламидиозу: Поскольку хламидийная инфекция может вызывать повреждение труб без очевидных симптомов, этот анализ крови проверяет наличие антител к хламидиозу. Положительный результат может указывать на перенесенную инфекцию, которая могла повлиять на трубы.
ЭКО часто рекомендуется женщинам с заблокированными или сильно поврежденными фаллопиевыми трубами, так как это полностью исключает необходимость в трубах. При ЭКО яйцеклетки извлекаются из яичников, оплодотворяются спермой в лаборатории, а полученные эмбрионы переносятся непосредственно в матку. ЭКО считается наиболее эффективным методом лечения трубного фактора бесплодия, особенно в случаях серьезного или необратимого повреждения. Женщины с одной заблокированной трубой все еще могут попытаться забеременеть естественным путем, но ЭКО предоставляет альтернативу, если другие попытки не увенчались успехом.
3- Физические проблемы с маткой
Физические аномалии или структурные проблемы в матке являются еще одним существенным фактором женского бесплодия. Матка или лоно обеспечивает среду для имплантации эмбриона и роста развивающегося плода. Структурные проблемы с маткой могут нарушить имплантацию оплодотворенной яйцеклетки, повлиять на развитие эмбриона или увеличить риск выкидыша. Эти проблемы часто называют бесплодием, связанным с маточным фактором, и они могут повлиять как на способность к зачатию, так и на вероятность сохранения здоровой беременности.
Типы структурных проблем матки и их влияние на фертильность
Существует несколько типов физических проблем, которые могут повлиять на матку и привести к бесплодию. Каждое состояние имеет уникальные эффекты на фертильность в зависимости от его местоположения, тяжести и основной причины. Наиболее распространенные структурные проблемы матки, связанные с бесплодием, включают:
1. Фибромиомы (лейомиомы матки):
Фибромы — это нераковые новообразования из мышечной и фиброзной ткани, которые развиваются в матке или на ее стенках. Хотя фибромы встречаются довольно часто, поражая до 70–80% женщин к 50 годам, они не всегда вызывают бесплодие. Влияние фибромиом на фертильность зависит от их размера, количества и расположения в матке. Субмукозные фибромиомы, которые растут в полости матки, с большей вероятностью будут мешать имплантации или развитию эмбриона. Крупные фибромиомы или множественные фибромиомы также могут изменять форму полости матки или блокировать маточные трубы, что еще больше затрудняет зачатие. Фибромиомы также могут повышать риск выкидыша, преждевременных родов и осложнений во время беременности в зависимости от их размера и расположения.
2. Полипы матки:
Полипы матки — это небольшие доброкачественные наросты, которые возникают из слизистой оболочки матки (эндометрия). Хотя полипы обычно не являются раковыми, они могут препятствовать фертильности, блокируя прохождение спермы, предотвращая имплантацию или нарушая кровоснабжение имплантированного эмбриона. Полипы могут быть особенно проблематичными, если они расположены в непосредственной близости от места, где обычно имплантируется эмбрион. В таких случаях они могут помешать успешной беременности или увеличить риск раннего выкидыша.
3. Врожденные аномалии матки:
Это структурные аномалии матки, присутствующие с рождения, вызванные проблемами развития в формировании мюллеровых протоков, которые дают начало матке, фаллопиевым трубам и верхней части влагалища. Врожденные аномалии матки могут принимать одну из следующих форм:
Двурогая матка: Матка имеет форму сердца с глубоким углублением наверху, что создает две полости. Двурогая матка может увеличить риск выкидыша, преждевременных родов и аномального положения плода.
Матка с перегородкой: Фиброзная или мышечная перегородка (стенка) разделяет полость матки частично или полностью. Это состояние связано с более высокими показателями выкидышей и неудач имплантации, поскольку перегородка может иметь сниженное кровоснабжение, что делает ее менее благоприятной для имплантации эмбриона.
Однорогая матка: Формируется только половина матки, что часто приводит к уменьшению полости матки. Это может привести к трудностям в поддержании беременности, с более высоким риском выкидыша и преждевременных родов.
Дидельфис Матка: Это редкое состояние, также известное как «двойная матка», возникает, когда формируются две отдельные полости матки. Хотя зачатие возможно, беременность может быть более рискованной из-за ограниченного пространства матки.
Врожденные аномалии матки часто способствуют повторным выкидышам, а также могут затруднить зачатие у женщин, особенно если форма матки препятствует правильной имплантации.
4. Внутриматочные спайки (синдром Ашермана):
Внутриматочные спайки — это полосы рубцовой ткани, которые образуются внутри матки, часто в результате травмы слизистой оболочки матки. Обычно они вызваны операциями на матке, такими как расширение и выскабливание (D&C), или инфекциями. Синдром Ашермана может привести к частичной или полной непроходимости полости матки, что может помешать имплантации или привести к повторному выкидышу. В тяжелых случаях спайки могут полностью предотвратить менструацию (аменорея). Женщины с синдромом Ашермана могут испытывать скудные или отсутствующие менструации, тазовые боли и бесплодие, особенно если спайки нарушают нормальную функцию матки.
5. Аденомиоз:
Аденомиоз возникает, когда эндометриальная ткань (слизистая оболочка матки) прорастает в мышечную стенку матки. Это состояние может вызвать утолщение, увеличение матки и привести к болезненным или обильным менструациям, тазовым болям и бесплодию. Аденомиоз обычно связан с неудачами имплантации и повышенным риском выкидыша. Хотя точная причина бесплодия при аденомиозе до конца не изучена, считается, что аномальный рост эндометриальной ткани в мышечной стенке нарушает нормальное функционирование матки.
6. Проблемы с эндометрием:
Толщина и качество эндометриальной выстилки имеют решающее значение для успешной имплантации эмбриона. В некоторых случаях у женщин эндометриальная выстилка может быть слишком тонкой или не развиваться должным образом, часто из-за гормонального дисбаланса, приема определенных лекарств или предыдущих операций на матке. Тонкий эндометрий может снизить вероятность имплантации, поскольку он может не обеспечить необходимую поддержку для прикрепления и развития эмбриона.
Симптомы структурных проблем матки
В то время как у некоторых женщин со структурными проблемами матки симптомы могут отсутствовать, у других могут наблюдаться следующие симптомы:
• Нерегулярные или обильные менструальные кровотечения (обычно при фибромиомах, полипах и аденомиозе)
• Болезненные менструации или боли в области таза
• Повторяющаяся потеря беременности или выкидыш
• Трудности с зачатием, несмотря на регулярную овуляцию и здоровье спермы
• Боль во время полового акта
Поскольку симптомы могут быть неявными или совпадать с симптомами других заболеваний, структурные проблемы матки часто диагностируются только после того, как женщина обращается за помощью по поводу бесплодия или повторяющихся выкидышей.
Диагностика структурных проблем матки
Для диагностики структурных проблем в матке часто используют комбинацию визуализирующих исследований и, при необходимости, малоинвазивных процедур.
УЗИ: Трансвагинальное УЗИ — это инструмент визуализации первой линии для оценки структуры матки. Он может определять фибромиомы, полипы, врожденные аномалии и аденомиоз. В некоторых случаях 3D-УЗИ может обеспечить более детальное представление о форме матки.
Гистеросальпингография (ГСГ): Эта рентгенологическая процедура включает введение контрастного вещества в матку для определения формы полости матки и проверки наличия непроходимости или спаек в фаллопиевых трубах.
Соногистерография: Солевой раствор вводится в матку во время УЗИ, чтобы обеспечить более четкое изображение полости матки. Этот метод может помочь обнаружить полипы, фибромиомы и спайки.
Магнитно-резонансная томография (МРТ): МРТ обеспечивает получение изображений матки с высоким разрешением и особенно полезна для диагностики аденомиоза, врожденных аномалий и глубоких миом матки.
Гистероскопия: Гистероскопия заключается в введении тонкого, освещенного зонда через шейку матки для непосредственного осмотра внутренней части матки. Это позволяет врачу визуально осмотреть полость матки на предмет полипов, фибром или спаек и, при необходимости, удалить или вылечить их во время той же процедуры.
Лапароскопия: Лапароскопия — это минимально инвазивная хирургическая процедура, которая позволяет врачу осмотреть внешнюю часть матки и окружающие ее структуры, такие как маточные трубы и яичники. Это особенно полезно для выявления эндометриоза или спаек в области таза, которые могут повлиять на фертильность.
4- Проблемы с шейкой матки
Проблемы с шейкой матки могут существенно повлиять на фертильность женщины, поскольку шейка матки играет важную роль в пути сперматозоидов к яйцеклетке. Шейка матки — это нижняя часть матки, которая соединяется с влагалищем и служит воротами для сперматозоидов, которые проникают в матку и движутся вверх к фаллопиевым трубам, где обычно происходит оплодотворение. Проблемы с шейкой матки, которые мешают функционированию или структуре шейки матки, могут помешать сперматозоидам достичь яйцеклетки, снизить вероятность имплантации или увеличить риск потери беременности.

Типы проблем шейки матки и их влияние на фертильность
Существует несколько типов заболеваний шейки матки, которые могут повлиять на фертильность:
1. Аномалии цервикальной слизи:
Цервикальная слизь, вырабатываемая железами шейки матки, имеет решающее значение для облегчения движения сперматозоидов. Во время овуляции цервикальная слизь становится тонкой, эластичной и скользкой (похожей на консистенцию яичного белка), что облегчает сперматозоидам перемещение через шейку матки в матку. Когда цервикальная слизь слишком густая, скудная или враждебная (неблагоприятная для сперматозоидов), она может препятствовать движению сперматозоидов или убивать их до того, как они достигнут яйцеклетки. Это состояние иногда называют «враждебной цервикальной слизью», и оно часто возникает из-за гормонального дисбаланса, инфекций, приема определенных лекарств или сопутствующих заболеваний. Недостаточное или некачественное количество цервикальной слизи также может помешать сперматозоидам выживать достаточно долго, чтобы достичь яйцеклетки, что снижает вероятность оплодотворения.
2. Стеноз цервикального канала (сужение цервикального канала):
Стеноз шейки матки — это состояние, при котором цервикальный канал становится аномально узким или закрытым, что затрудняет прохождение спермы. Это состояние может быть врожденным (присутствующим с рождения) или приобретенным из-за хирургических операций, инфекций, травм или лучевой терапии. В тяжелых случаях стеноз шейки матки может полностью препятствовать прохождению спермы, фактически препятствуя естественному зачатию. Стеноз шейки матки также может привести к нарушениям менструального цикла и болям, поскольку менструальная кровь может с трудом проходить через суженную шейку матки. В случаях тяжелого стеноза могут быть рекомендованы вспомогательные репродуктивные методы, такие как внутриматочная инсеминация (ВМИ) или экстракорпоральное оплодотворение (ЭКО), чтобы обойти шейку матки.
3. Инфекции и воспаления шейки матки:
Инфекции шейки матки, такие как цервицит (воспаление шейки матки) или инфекции, передающиеся половым путем (ИППП), такие как хламидиоз и гонорея, могут повлиять на фертильность. Воспаление и инфекция шейки матки могут изменить качество цервикальной слизи, сделав ее менее благоприятной для спермы. В некоторых случаях нелеченные инфекции могут привести к развитию рубцовой ткани, которая может сузить цервикальный канал. Инфекции также могут распространяться вверх, приводя к воспалительным заболеваниям органов малого таза (ВЗОМТ), которые могут еще больше повлиять на фертильность, вызывая рубцевание и закупорку фаллопиевых труб.
4. Истмико-цервикальная недостаточность (несостоятельность шейки матки):
Цервикальная недостаточность, также известная как несостоятельность шейки матки, возникает, когда шейка матки слишком слаба, чтобы оставаться закрытой во время беременности. Хотя это состояние напрямую не препятствует зачатию, оно может привести к выкидышу, особенно во втором триместре, так как шейка матки может начать преждевременно раскрываться. Цервикальная недостаточность может быть вызвана генетическими факторами, предыдущими операциями на шейке матки (например, процедурой LEEP или конической биопсией), травмой при родах или врожденными аномалиями. Женщины с этим состоянием часто сталкиваются с повторной потерей беременности и могут нуждаться в медицинских вмешательствах для поддержки шейки матки во время беременности.
5. Предыдущие операции или процедуры на шейке матки:
Некоторые процедуры на шейке матки, такие как LEEP (петлевая электрохирургическая эксцизия) или коническая биопсия, используются для удаления предраковых клеток из шейки матки, но иногда могут влиять на фертильность. Эти процедуры могут ослабить шейку матки или вызвать рубцевание, что может привести к цервикальной недостаточности или стенозу. Хотя большинство женщин сохраняют фертильность после этих процедур, те, у кого возникают осложнения, могут столкнуться с более высоким риском бесплодия, повторной потери беременности или преждевременных родов. В некоторых случаях рубцы на шейке матки после операции могут повлиять на выработку слизи или затруднить прохождение спермы.
6. Антиспермальные антитела в цервикальной слизи:
В редких случаях иммунная система женщины может вырабатывать антитела против сперматозоидов, воспринимая их как чужеродных захватчиков. Эти антитела могут присутствовать в цервикальной слизи и могут нарушать движение сперматозоидов, повреждать сперму или не давать сперме достичь матки. Наличие антиспермальных антител в цервикальной слизи может привести к так называемому «иммунологическому бесплодию», которое может потребовать специальных методов лечения, таких как ВМИ или ЭКО, чтобы помочь обойти шейку матки и повысить шансы на оплодотворение.
Диагностика проблем шейки матки при бесплодии
Диагностика бесплодия, связанного с шейкой матки, обычно включает ряд тестов и оценок. Гинекологический осмотр позволяет врачу оценить размер, форму и положение шейки матки, а также проверить наличие видимых отклонений или признаков воспаления. Иногда может быть назначен посткоитальный тест, если есть подозрение на враждебную слизь. В этом тесте образец цервикальной слизи собирается после полового акта для изучения движения сперматозоидов в слизи. Этот тест помогает оценить, поддерживает или подавляет цервикальная слизь движение сперматозоидов, хотя сегодня он используется реже из-за переменных результатов.
HSG — это рентгенологическая процедура, которая использует контрастное вещество для оценки формы матки и проходимости (открытости) цервикального канала и фаллопиевых труб. Она помогает обнаружить любые структурные блокировки в шейке матки. Цервикальные культуры могут быть выполнены для выявления инфекций, в то время как биопсия шейки матки может оценить наличие любых аномальных или предраковых клеток. Эти тесты могут помочь выявить инфекции или рубцы, которые могут влиять на фертильность.
Ультразвуковое исследование может использоваться для оценки структуры и длины шейки матки, особенно в случаях, когда подозревается истмико-цервикальная недостаточность. Трансвагинальное УЗИ часто используется для контроля длины шейки матки во время беременности у женщин с анамнезом истмико-цервикальной недостаточности.
5- Возраст
Возраст является одним из наиболее значимых факторов, влияющих на женскую фертильность. С возрастом фертильность женщины естественным образом снижается из-за изменений как в количестве, так и в качестве ее яйцеклеток, а также изменений в ее репродуктивной системе, которые влияют на зачатие и беременность. Снижение фертильности обычно начинается в конце 20-х - начале 30-х годов и значительно ускоряется после 35 лет. К тому времени, когда женщина достигает 40 лет, вероятность естественного зачатия значительно снижается, а риск осложнений увеличивается. По мере увеличения возраста женщины происходят следующие изменения:
1. Снижение количества яйцеклеток (резерв яичников)
Женщины рождаются со всеми яйцеклетками, которые у них когда-либо будут, примерно 1-2 миллиона на момент рождения. К половому созреванию это число уже уменьшается примерно до 300 000 - 400 000, и с каждым менструальным циклом все больше яйцеклеток истощается. К концу 30-х годов количество оставшихся яйцеклеток (известных как овариальный резерв) быстро уменьшается. Когда женщина приближается к менопаузе, как правило, около начала 50-х годов, остается очень мало, если вообще остается, жизнеспособных яйцеклеток. Уменьшение овариального резерва влияет на способность женщины к зачатию, так как меньшее количество яйцеклеток означает меньше возможностей для оплодотворения. Сокращение количества яйцеклеток также ограничивает эффективность методов лечения бесплодия, таких как экстракорпоральное оплодотворение (ЭКО), поскольку яичники могут не вырабатывать достаточное количество яйцеклеток в ответ на стимуляцию.
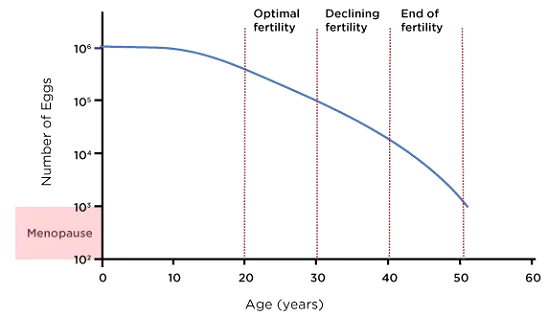
2. Снижение качества яиц
С возрастом уменьшается не только количество яйцеклеток, но и их качество. Качество яйцеклеток относится к генетической и хромосомной целостности яйцеклетки. По мере того, как женщины стареют, яйцеклетки с большей вероятностью накапливают хромосомные аномалии, увеличивая вероятность генетических нарушений, таких как синдром Дауна, и снижая шансы на успешное зачатие. Хромосомные аномалии также увеличивают риск выкидыша, особенно у женщин старше 35 лет. Исследования показывают, что частота выкидышей у женщин в возрасте около 20 лет составляет около 10-15%, но эта частота возрастает до около 35% у женщин в возрасте около 40 лет.
Не только генетические проблемы распространены в ооцитах в более старших возрастных группах, но и цитоплазматические органеллы также теряют свою функцию с увеличением возраста. Особенно митохондриальная функция жизненно важна для роста и развития клеток, и стареющие митохондрии могут не обеспечивать необходимый баланс между производством энергии и окислительным повреждением внутри ооцитов. Некоторые методы лечения нового поколения, такие как «Митохондриальная заместительная терапия», могут быть полезны в случаях, когда старение ооцитов вызывает беспокойство во время лечения бесплодия. Снижение качества яйцеклеток является важной причиной того, что показатели беременности и живорождения снижаются с возрастом, даже при использовании лечения бесплодия.
3. Повышенный риск проблем с репродуктивным здоровьем
С возрастом у женщин повышается вероятность развития заболеваний, которые могут повлиять на фертильность, включая эндометриоз, фибромиому матки и хронические осложнения воспалительных заболеваний органов малого таза. Эти проблемы со здоровьем не только влияют на шансы зачатия, но и могут увеличить риск осложнений беременности и выкидыша.
4. Сниженная восприимчивость матки
С возрастом матка также может претерпевать изменения, которые влияют на ее способность поддерживать беременность. Эндометриальный слой, который утолщается с каждым циклом, чтобы подготовиться к потенциальному эмбриону, может не развиваться так оптимально, как раньше. Это изменение может снизить вероятность успешной имплантации, даже если присутствует здоровый эмбрион. Сосудистая система в матке также может быть затронута возрастом, уменьшая приток крови к эндометриальному слою. Адекватный приток крови необходим для восприимчивой матки, которая может поддерживать эмбрион, поэтому уменьшение притока крови может снизить фертильность и увеличить риск ранней потери беременности.
5. Повышенный риск осложнений беременности
Женщины старшего возраста, которые забеременели естественным путем или с помощью, подвергаются более высокому риску осложнений беременности. К этим осложнениям относятся:
Гестационный диабет: женщины старше 35 лет подвержены повышенному риску развития гестационного диабета, который может повлиять на здоровье как матери, так и плода.
Гипертония и преэклампсия: высокое кровяное давление и преэклампсия (потенциально опасное осложнение беременности, характеризующееся высоким кровяным давлением) чаще встречаются у матерей старшего возраста.
Предлежание плаценты: у женщин старше 35 лет повышен риск предлежания плаценты — состояния, при котором плацента закрывает шейку матки, что может привести к осложнениям во время родов.
Преждевременные роды: женщины старше 35 лет подвержены более высокому риску преждевременных родов, что может повлиять на здоровье ребенка.
Эти осложнения беременности, хотя и не влияют напрямую на способность к зачатию, подчеркивают дополнительные риски для здоровья, с которыми сталкиваются женщины, пытающиеся забеременеть в более старшем возрасте. Возраст влияет не только на естественное зачатие, но и на показатели успешности вспомогательных репродуктивных технологий, таких как ЭКО. Женщины до 35 лет, как правило, имеют более высокие показатели успешности ЭКО по сравнению с женщинами старше 40 лет. К 43 годам показатель успешности ЭКО с собственными яйцеклетками женщины значительно падает, в основном из-за уменьшения количества и качества яйцеклеток. Чтобы увеличить свои шансы, некоторые женщины в возрасте предпочитают использовать донорские яйцеклетки от молодой женщины, что значительно повышает показатели успешности, поскольку донорские яйцеклетки, как правило, более высокого качества. Однако процесс донорства яйцеклеток является дорогостоящим и требует тщательного рассмотрения и подготовки.
Варианты сохранения фертильности: заморозка яйцеклеток и эмбрионов
В связи со снижением фертильности, связанным с возрастом, некоторые женщины предпочитают сохранить свою фертильность с помощью заморозки яйцеклеток или эмбрионов (криоконсервации) в молодом возрасте, особенно если они планируют отложить беременность.
Заморозка яйцеклеток: этот процесс включает стимуляцию яичников для производства нескольких яйцеклеток, которые затем извлекаются и замораживаются для будущего использования. Заморозка яйцеклеток может позволить женщинам использовать более молодые, здоровые яйцеклетки, когда они будут готовы к зачатию, увеличивая их шансы на успешную беременность в более позднем возрасте.
Заморозка эмбрионов: Подобно заморозке яйцеклеток, этот процесс включает оплодотворение извлеченных яйцеклеток спермой перед заморозкой. Этот вариант часто выбирают женщины, которые находятся в серьезных отношениях и хотят иметь эмбрионы, готовые к имплантации в будущем.
Эти методы предоставляют возможности женщинам, желающим отсрочить беременность, сохранив при этом качество своих яйцеклеток или эмбрионов. Хотя возраст является основным фактором фертильности, такие медицинские достижения, как ВРТ, заморозка яйцеклеток и заморозка эмбрионов, предоставляют возможности, помогающие женщинам забеременеть в более позднем возрасте. Понимание влияния возраста на фертильность может помочь женщинам сделать осознанный репродуктивный выбор и обратиться за помощью на раннем этапе, если они планируют забеременеть в более старшем возрасте.
6- Проблемы с иммунной системой
Иммунные проблемы могут существенно влиять на фертильность у женщин, часто приводя к необъяснимому бесплодию, повторной потере беременности или осложнениям во время беременности. Иммунная система предназначена для защиты организма от инфекций и чужеродных захватчиков, но в некоторых случаях иммунные реакции могут мешать фертильности, нацеливаясь на репродуктивные клетки, ткани или даже эмбрион. Эти связанные с иммунитетом проблемы фертильности могут быть результатом аутоиммунных заболеваний, иммунных реакций на сперму или эмбрионы или аномальной активации иммунной системы.
1. Аутоиммунные заболевания и бесплодие
При аутоиммунных расстройствах иммунная система ошибочно атакует собственные ткани организма, как будто это чужеродные захватчики. Несколько аутоиммунных состояний связаны с бесплодием:
Системная красная волчанка (СКВ): Волчанка — это аутоиммунное заболевание, которое может вызывать воспаление во всем организме, включая репродуктивные органы. Женщины с волчанкой могут испытывать нарушения менструального цикла, повторяющиеся выкидыши или преждевременные роды из-за атак иммунной системы на матку или плаценту.
Антифосфолипидный синдром (APS): APS — это аутоиммунное заболевание, при котором иммунная система вырабатывает антитела против фосфолипидов, молекул в клеточных мембранах, и это часто связано с повторным выкидышем. Эти антифосфолипидные антитела могут привести к образованию тромбов в плаценте, что приводит к прекращению кровоснабжения плода и вызыванию выкидыша. APS также связан с другими осложнениями, такими как преэклампсия и преждевременные роды.
Тиреоидит Хашимото и болезнь Грейвса: оба являются аутоиммунными заболеваниями щитовидной железы, при которых иммунная система атакует щитовидную железу, либо снижая (Хашимото), либо увеличивая (Брейвс) выработку гормонов щитовидной железы. Гормоны щитовидной железы играют важную роль в регуляции менструального цикла и поддержании беременности. Женщины с заболеваниями щитовидной железы часто испытывают нарушения менструального цикла, проблемы с овуляцией и более высокий риск выкидыша.
Ревматоидный артрит (РА) и другие аутоиммунные заболевания: РА и подобные аутоиммунные заболевания могут вызывать воспалительные состояния, которые мешают овуляции, имплантации эмбриона и поддержанию беременности. Кроме того, некоторые лекарства, используемые для лечения аутоиммунных заболеваний, могут негативно влиять на фертильность.
2. Антиспермальные антитела
В некоторых случаях иммунная система женщины может вырабатывать антитела, которые специально нацелены на сперму. Такая реакция может возникнуть, если сперма подвергается воздействию иммунной системы из-за травмы, инфекции или хирургического вмешательства. Антитела могут нарушить подвижность сперматозоидов (затрудняя их движение), связываться с поверхностью сперматозоидов или даже полностью уничтожать сперму, тем самым предотвращая оплодотворение. Антиспермальные антитела обычно находятся в цервикальной слизи, но они также могут присутствовать в других областях репродуктивной системы. Женщинам с антиспермальными антителами могут потребоваться такие методы лечения, как внутриматочная инсеминация (ВМИ) или экстракорпоральное оплодотворение (ЭКО), чтобы обойти цервикальную слизь и повысить шансы на зачатие.
3. Анти-овариальные антитела
Антиовариальные антитела — это антитела, которые атакуют ткань яичников, нацеливаясь на такие компоненты, как яйцеклетки, рецепторы фолликулостимулирующего гормона (ФСГ) или структуры, которые поддерживают развитие яйцеклеток. Этот иммунный ответ может нарушить функцию яичников, снизить качество яйцеклеток и привести к раннему старению или отказу яичников (известному как первичная недостаточность яичников или ПНЯ). Женщины с антиовариальными антителами могут испытывать нерегулярные менструальные циклы, ановуляцию (отсутствие овуляции) или снижение овариального резерва, все это может снизить фертильность и сделать зачатие более сложным. Аутоиммунная недостаточность яичников иногда связана с другими аутоиммунными заболеваниями, такими как болезнь Аддисона, волчанка или заболевания щитовидной железы.
4. Эндометриоз и воспаление
Эндометриоз — это состояние, при котором ткань, похожая на слизистую оболочку матки (эндометрий), разрастается за пределами матки, часто на яичниках, фаллопиевых трубах и других органах малого таза. Хотя эндометриоз не является строго аутоиммунным заболеванием, было обнаружено, что он связан с дисфункцией иммунной системы и хроническим воспалением. У женщин с эндометриозом иммунная система не может очистить неправильно расположенную эндометриальную ткань, что приводит к постоянному воспалению. Эта воспалительная среда может влиять на качество яйцеклеток, нарушать овуляцию и создавать спайки (рубцовую ткань), которые блокируют или повреждают фаллопиевы трубы. Воспаление и иммунная активность, связанные с эндометриозом, также могут создавать враждебную среду для спермы, яйцеклеток и эмбрионов, что затрудняет достижение успешной беременности.
5. Естественные клетки-киллеры (NK) и неудача имплантации
Естественные клетки-киллеры (NK) — это иммунные клетки, которые играют важную роль в защитных механизмах организма, включая регулирование иммунных реакций в матке. При типичной беременности маточные NK-клетки помогают поддерживать имплантацию, способствуя притоку крови к развивающемуся эмбриону. Однако у некоторых женщин может быть повышенный уровень NK-клеток или аномально активированных NK-клеток, которые нацелены на эмбрион и атакуют его, что приводит к неудаче имплантации или ранней потере беременности. Повышенная активность NK-клеток связана с повторными выкидышами и может способствовать необъяснимому бесплодию. Тестирование на активность NK-клеток является спорным, поскольку не все исследователи согласны с ее влиянием на фертильность, но некоторые специалисты по фертильности могут предлагать иммуномодулирующие методы лечения, такие как стероиды или внутривенный иммуноглобулин (ВВИГ), для снижения активности NK-клеток и улучшения успешности имплантации.
6. Дисбаланс цитокинов и воспалительная реакция
Цитокины — это небольшие белки, вырабатываемые иммунными клетками, которые играют роль в клеточной сигнализации и иммунной регуляции. На ранних сроках беременности сбалансированная цитокиновая среда необходима для поддержки имплантации эмбриона и раннего развития плода. Однако дисбаланс цитокинов, особенно увеличение провоспалительных цитокинов, может нарушить этот процесс. У женщин с иммуноопосредованным бесплодием повышенный уровень воспалительных цитокинов может создать неблагоприятную среду в матке, снижая шансы имплантации эмбриона или увеличивая риск выкидыша. Такие состояния, как аутоиммунные заболевания, инфекции или хроническое воспаление, могут привести к дисбалансу цитокинов, что может способствовать бесплодию или повторной потере беременности.
7. Иммунный ответ на плаценту
Плацента, которая питает развивающийся плод, имеет решающее значение для успешной беременности. Во время нормальной беременности материнская иммунная система толерантна к плаценте, которая имеет генетический материал как от матери, так и от отца. Однако у некоторых женщин иммунная система может рассматривать плаценту как чужеродную и инициировать иммунный ответ против нее. Этот иммунный ответ может ограничить приток крови к плаценте, увеличивая риск выкидыша, преэклампсии, задержки внутриутробного развития и других осложнений беременности. Такие состояния, как АФС (антифосфолипидный синдром), являются классическими примерами, когда иммунные ответы могут мешать функции плаценты, что приводит к потере беременности.
8. Иммунологическая дисфункция имплантации
У некоторых женщин с необъяснимым бесплодием может быть так называемая иммунологическая дисфункция имплантации. Этот термин относится к сверхактивной или неадекватной иммунной реакции, которая не позволяет эмбриону успешно имплантироваться в матку, даже если и эмбрион, и слизистая оболочка матки здоровы. Иммунологическая дисфункция имплантации все еще является областью исследований, но считается, что она связана с аномальной активностью иммунных клеток, включая NK-клетки, Т-клетки и макрофаги, или дисбалансом иммуномодулирующих факторов в матке. Варианты лечения все еще разрабатываются, но некоторые специалисты по фертильности могут использовать кортикостероиды, внутривенные иммуноглобулины или другие иммуномодулирующие терапии, чтобы попытаться улучшить успешность имплантации.
Диагностическое тестирование на иммуноопосредованное бесплодие
Тестирование на иммуноопосредованное бесплодие может включать несколько подходов в зависимости от предполагаемой иммунной проблемы:
Анализы крови: Анализы крови позволяют обнаружить специфические антитела (например, антиспермальные антитела, антиовариальные антитела, антифосфолипидные антитела) и измерить уровни или активность иммунных клеток.
Анализы NK-клеток: Эти тесты оценивают уровень и активность естественных клеток-киллеров в крови или матке, хотя их клиническая ценность до сих пор остается предметом споров.
Тестирование профиля цитокинов: Этот тест измеряет уровни провоспалительных и противовоспалительных цитокинов для оценки иммунного баланса, особенно у женщин с привычным невынашиванием беременности.
Гистероскопия или биопсия: Для оценки воспаления или иммунной активности непосредственно в матке может быть проведена гистероскопия (осмотр матки с помощью камеры) или биопсия эндометрия.
Варианты лечения иммунозависимого бесплодия
Лечение иммунозависимого бесплодия направлено на устранение конкретной иммунной проблемы и повышение шансов на успешную беременность:
Иммуномодулирующие препараты:
• Кортикостероиды: Низкие дозы стероидов, таких как преднизон, могут использоваться для снижения иммунной активности и воспаления, особенно в случаях повышения уровня NK-клеток или иммунологической неудачи имплантации.
• Внутривенный иммуноглобулин (ВВИГ): В некоторых случаях ВВИГ используется для подавления аномальных иммунных реакций, особенно у женщин с привычным невынашиванием беременности или повышением уровня NK-клеток, хотя его применение все еще находится на экспериментальном уровне.
• Низкомолекулярный гепарин (НМГ) и аспирин: В случаях антифосфолипидного синдрома или нарушений свертываемости крови препараты, разжижающие кровь, такие как гепарин и аспирин, могут снизить риск образования тромбов, поддерживая здоровье плаценты и снижая риск выкидыша.
Антибиотики при инфекциях: в случаях цервицита или неспецифических инфекций антибиотики могут уменьшить воспаление в репродуктивной системе, потенциально улучшая фертильность.
Вспомогательные репродуктивные технологии (ВРТ):
В случаях, когда проблемы с иммунитетом мешают естественному зачатию, такие варианты ВРТ, как ЭКО, могут обойти некоторые иммунные барьеры, позволяя оплодотворению произойти вне организма. Такие методы, как интрацитоплазматическая инъекция сперматозоида (ИКСИ), могут использоваться в случаях наличия антиспермальных антител, а перенос эмбриона может обойти враждебную цервикальную слизь или аномальные иммунные реакции в шейке матки.
7- Дефекты тромбофилии
Тромбофилия, состояние, характеризующееся повышенной склонностью к образованию тромбов, может существенно влиять на женскую фертильность, в частности, влияя на имплантацию и увеличивая риск осложнений беременности. Тромбофилия может быть как наследственной (генетической), так и приобретенной, и часто связана с нарушениями в механизмах свертывания крови. Хотя сама по себе тромбофилия не препятствует зачатию напрямую, она может создать среду, которая затрудняет развитие беременности, что приводит к повторным выкидышам, осложнениям во время беременности и, в некоторых случаях, проблемам с имплантацией.
Типы тромбофилии и их влияние на фертильность
Тромбофилия может быть результатом генетических мутаций или приобретенных состояний, которые влияют на свертываемость крови. Распространенные типы тромбофилии, связанные с бесплодием и потерей беременности, включают:
Наследственные тромбофилии:
а) Фактор V Лейденская мутация: Эта мутация делает кровь более склонной к свертыванию, изменяя функцию фактора свертывания V, белка в крови. Женщины с этой мутацией имеют
б) Мутация гена протромбина (G20210A): Эта мутация увеличивает уровень протромбина, другого белка свертывания крови, что приводит к более высокому риску образования тромбов и связанной с этим потери беременности.
в) Дефицит протеина C, протеина S и антитромбина: Это редкие наследственные заболевания, которые снижают способность организма регулировать свертываемость. Дефицит этих белков увеличивает риск образования аномальных тромбов и осложнений во время беременности.
Приобретенная тромбофилия:
а) Антифосфолипидный синдром (АФС): АФС — это аутоиммунное заболевание, при котором иммунная система вырабатывает антитела против фосфолипидов, молекул в клеточных мембранах. АФС тесно связан с бесплодием и привычным выкидышем, поскольку антитела приводят к образованию тромбов в плаценте, что снижает приток крови к плоду и приводит к потере беременности.
б) Гипергомоцистеинемия: Повышенный уровень гомоцистеина (аминокислоты) в крови может увеличить риск образования тромбов и связан с потерей беременности и проблемами с плацентой. Гипергомоцистеинемия иногда связана с мутациями гена MTHFR.
Как тромбофилия влияет на имплантацию и раннюю беременность
Свертывание крови играет важную роль на ранних сроках беременности, особенно в формировании плаценты, которая поддерживает эмбрион. Тромбофилия может мешать этим процессам несколькими способами.
Тромбофилия может привести к образованию микротромбов в кровеносных сосудах матки и плаценты. Эти тромбы могут ограничить приток крови к эндометрию (слизистой оболочке матки) и развивающейся плаценте, лишая эмбрион необходимых питательных веществ и кислорода. На ранних стадиях беременности недостаточный приток крови может помешать правильной имплантации и привести к ранней потере беременности.
Имплантация, при которой эмбрион прикрепляется к эндометрию, требует здорового кровоснабжения и хорошо функционирующих кровеносных сосудов. Если свертывание крови нарушает приток крови к матке, это может создать неблагоприятную среду для эмбриона, снижая вероятность успешной имплантации. Женщины с тромбофилией могут испытывать необъяснимое бесплодие из-за повторяющихся неудач имплантации, даже если оплодотворение произошло.
Тромбофилия — известный фактор риска повторного выкидыша, определяемый как две или более последовательных потери беременности. Сгустки крови, которые образуются в плацентарных кровеносных сосудах, могут привести к плацентарной недостаточности, когда плацента не может адекватно поддерживать развивающийся эмбрион или плод. Это может привести к:
Ранняя потеря беременности: У многих женщин с тромбофилией случается выкидыш в течение первого триместра, поскольку в крошечных кровеносных сосудах плаценты образуются тромбы, перекрывающие приток крови к эмбриону.
Потеря во втором триместре: Тромбофилия также может привести к потере беременности во втором триместре из-за плохого развития плаценты и кровотока, что может привести к задержке роста плода или отслойке плаценты (когда плацента отделяется от стенки матки).
Мертворождение: В редких случаях тромбофилия может способствовать мертворождению, если приток крови к плоду резко ограничен на поздних стадиях беременности.
Диагностическое тестирование на тромбофилию при бесплодии
Женщины, которые сталкиваются с повторной потерей беременности, необъяснимым бесплодием или осложнениями беременности, могут пройти тест на тромбофилию. Обычные тесты включают:
• Тесты на свертываемость крови: Эти тесты измеряют уровни факторов свертывания крови и белков, таких как фактор V Лейдена, протромбин, белок C, белок S и антитромбин.
• Тест на антифосфолипидные антитела: Этот тест проверяет наличие антифосфолипидных антител, которые связаны с АФС. Тестирование может включать антикардиолипиновые антитела, волчаночный антикоагулянт и антитела к бета-2 гликопротеину I.
• Уровень гомоцистеина: Повышенный уровень гомоцистеина связан с нарушениями свертываемости крови и может указывать на скрытую генетическую мутацию, например мутацию MTHFR.
При правильном лечении, включая антикоагулянтную терапию и тщательное наблюдение, многие женщины с тромбофилией могут успешно забеременеть и выносить здоровую беременность до срока. Ранняя диагностика и лечение являются ключом к снижению рисков, связанных с тромбофилией, и улучшению результатов фертильности.
8- Факторы образа жизни и воздействия окружающей среды
Факторы образа жизни существенно влияют на женскую фертильность, влияя на овуляцию, качество яйцеклеток, уровень гормонов и общее репродуктивное здоровье. Несколько ключевых факторов образа жизни, которые могут повлиять на фертильность, включают диету, вес, физическую активность, уровень стресса, курение, употребление алкоголя и воздействие токсинов окружающей среды.
1. Диета и питание
Хорошо сбалансированная диета, которая обеспечивает необходимыми питательными веществами, жизненно важна для репродуктивного здоровья. Определенные питательные вещества, витамины и минералы поддерживают овуляцию, выработку гормонов и качество яйцеклеток. Неправильное питание или определенные дефициты могут нарушить эти процессы, влияя на фертильность:
Антиоксиданты: продукты, богатые антиоксидантами (такими как витамины С и Е, фолиевая кислота и бета-каротин), помогают защитить яйца от окислительного стресса, который может ухудшить качество яиц.
Фолиевая кислота: этот витамин группы В имеет решающее значение для синтеза ДНК и деления клеток, что делает его незаменимым для качества яйцеклеток и развития эмбриона.
Железо: Дефицит железа может привести к проблемам с овуляцией, поскольку железо необходимо для кроветворения и транспорта кислорода.
Здоровые жиры: жирные кислоты омега-3, содержащиеся в рыбе, льняном семени и грецких орехах, помогают уменьшить воспаление и поддерживают выработку гормонов. Трансжиры, обычно встречающиеся в обработанных пищевых продуктах, могут негативно влиять на овуляцию, и их следует избегать.
Высокое содержание сахара и обработанных пищевых продуктов: рацион с высоким содержанием сахара и обработанных пищевых продуктов может привести к резистентности к инсулину и гормональному дисбалансу, что может повлиять на овуляцию.
Здоровая, богатая питательными веществами диета поддерживает регулярные менструальные циклы, улучшает качество яйцеклеток и создает благоприятные условия для зачатия.
2. Масса тела и фертильность
Масса тела оказывает существенное влияние на фертильность. Как недостаточный, так и избыточный вес могут привести к гормональному дисбалансу, который нарушает овуляцию и регулярность менструального цикла:
Недостаточный вес: Женщины с очень низким индексом массы тела (ИМТ) могут испытывать нерегулярные или отсутствующие менструации (аменорея) из-за низкого уровня эстрогена. Эстроген необходим для овуляции и поддержания здорового менструального цикла, а недостаточное количество жира в организме может ухудшить его выработку.
Избыточный вес/Ожирение: Избыточный вес, особенно в области живота, связан с гормональным дисбалансом и такими состояниями, как синдром поликистозных яичников (СПКЯ), которые могут препятствовать овуляции. Ожирение может привести к резистентности к инсулину, повышенному уровню андрогенов и снижению фертильности. Исследования показывают, что даже снижение веса 5-10% может улучшить овуляцию и повысить вероятность зачатия.
Поддержание здорового веса — один из наиболее эффективных способов оптимизации фертильности и улучшения репродуктивных результатов.
3. Физическая активность
Регулярная физическая активность поддерживает общее состояние здоровья, гормональную регуляцию и контроль веса. Однако влияние упражнений на фертильность может зависеть от их интенсивности:
• Умеренные упражнения: Умеренная, регулярная физическая активность может улучшить фертильность, регулируя вес, снижая стресс и улучшая приток крови к репродуктивным органам. Обычно рекомендуется женщинам, пытающимся забеременеть.
• Чрезмерные упражнения: Интенсивные, высокоэффективные упражнения могут привести к гормональному дисбалансу, особенно у женщин с низким содержанием жира в организме. Чрезмерные упражнения могут вызвать снижение уровня эстрогена, нарушить менструальный цикл и, в тяжелых случаях, привести к гипоталамической аменорее (отсутствию менструаций из-за недостаточной выработки гормонов).
Ключевым фактором поддержания репродуктивного здоровья является сбалансированный уровень физической активности, при этом особое внимание следует уделять умеренным и регулярным физическим упражнениям.
4. Стресс и эмоциональное благополучие
Хронический стресс может негативно влиять на фертильность, нарушая гормональный баланс и овуляцию. Высокий уровень стресса увеличивает выработку кортизола, гормона, который может влиять на репродуктивные гормоны, такие как ГнРГ (гонадотропин-рилизинг-гормон), который регулирует овуляцию. Стресс также связан с нездоровым поведением, таким как плохое питание, недостаток сна и физическая неактивность, что может еще больше повлиять на фертильность. Кроме того, эмоциональное воздействие стресса может усложнить зачатие и даже может способствовать циклу стресса и бесплодия. Практики осознанности, консультирование и методы управления стрессом, такие как йога, медитация или терапия, могут быть полезны для женщин, пытающихся забеременеть.
5. курение
Курение является одним из самых вредных факторов образа жизни, влияющих на фертильность. Табак содержит токсичные химические вещества, такие как никотин, окись углерода и смолы, которые могут влиять на репродуктивное здоровье несколькими способами:
• Качество яйцеклеток: курение ускоряет потерю яйцеклеток и ухудшает их качество, что приводит к более высокому риску хромосомных аномалий.
• Овуляция: Курильщики чаще испытывают проблемы с овуляцией, что затрудняет зачатие.
• Здоровье матки: курение влияет на приток крови к матке, потенциально создавая неблагоприятные условия для имплантации эмбриона.
• Ранняя менопауза: курящие женщины часто достигают менопаузы на 1–4 года раньше, чем некурящие, что сокращает их фертильное окно.
Даже пассивное курение может повлиять на фертильность. Отказ от курения — одно из самых полезных изменений, которые женщина может сделать, чтобы повысить свои шансы на зачатие.
6. Употребление алкоголя
Чрезмерное употребление алкоголя может нанести вред фертильности и исходу беременности:
• Овуляция и гормональный дисбаланс: чрезмерное употребление алкоголя может нарушить выработку гормонов, необходимых для овуляции и регулярности менструального цикла, что повышает риск бесплодия.
• Снижение показателей фертильности: исследования показывают, что у женщин, употребляющих большое количество алкоголя, может наблюдаться снижение показателей фертильности по сравнению с умеренно пьющими или непьющими.
• Риски во время беременности: употребление алкоголя может повлиять на раннюю беременность, увеличивая риск выкидыша и проблем с развитием плода.
Хотя умеренное употребление алкоголя может иметь минимальные последствия, женщинам, пытающимся забеременеть, обычно рекомендуется воздержаться от него или сократить его употребление.
7. Потребление кофеина
Хотя умеренное потребление кофеина (например, до 200 мг в день или около одной чашки кофе объемом 350 мл) обычно считается безопасным, высокое потребление кофеина может негативно сказаться на фертильности:
• Задержка зачатия: некоторые исследования показали, что высокое потребление кофеина может быть связано с задержкой зачатия или повышенным риском выкидыша.
• Снижение усвоения некоторых питательных веществ: чрезмерное употребление кофеина может препятствовать усвоению необходимых питательных веществ, таких как кальций и железо, которые важны для репродуктивного здоровья.
Большинство специалистов в области здравоохранения рекомендуют ограничить потребление кофеина при попытках забеременеть.
8. Экологические токсины и химическое воздействие
Воздействие токсинов окружающей среды, включая определенные химические вещества, загрязняющие вещества и вещества, нарушающие работу эндокринной системы, может повлиять на фертильность:
• Эндокринные разрушители: Химические вещества, такие как бисфенол А (БФА), фталаты и пестициды, могут имитировать или блокировать естественные гормоны, что приводит к гормональному дисбалансу, который нарушает овуляцию, менструальные циклы и общую репродуктивную функцию.
• Тяжелые металлы: воздействие тяжелых металлов, таких как свинец и ртуть, может нарушить функцию яичников, снизить качество яйцеклеток и нарушить менструальный цикл.
• Профессиональные риски: женщины, работающие в определенных отраслях, таких как сельское хозяйство, производство или лаборатории, могут подвергаться воздействию химических веществ и радиации, которые отрицательно влияют на фертильность.
Сокращение воздействия токсинов окружающей среды — например, отказ от пластиковой тары с БФА, выбор органических продуктов, когда это возможно, и минимизация использования определенных косметических средств — может помочь поддержать репродуктивное здоровье.
9. Режимы сна и циркадные ритмы
Неправильный режим сна и нерегулярный сон могут повлиять на фертильность, нарушая уровень гормонов, особенно репродуктивных гормонов, которые регулируют овуляцию и менструальные циклы:
• Мелатонин и репродуктивное здоровье: Мелатонин, гормон, связанный со сном, также действует как антиоксидант, защищающий яйцеклетки от повреждений. Женщины с недостаточным или некачественным сном могут испытывать снижение уровня мелатонина, что может повлиять на здоровье яйцеклеток.
• Сменная работа: у женщин, работающих в ночную смену или имеющих нерегулярный рабочий день, могут нарушаться циркадные ритмы, что может привести к нарушениям менструального цикла и снижению фертильности.
Поддержание постоянного режима сна и стремление спать по 7–8 часов в сутки может помочь поддержать гормональный баланс и репродуктивное здоровье.
10. Употребление наркотиков в рекреационных целях
Употребление наркотиков, таких как марихуана, кокаин и другие вещества, может иметь пагубные последствия для фертильности:
• Гормональный дисбаланс: многие рекреационные наркотики влияют на гормональные сигналы, необходимые для овуляции и регулярности менструального цикла.
• Качество яйцеклеток и овуляция: некоторые наркотики, особенно марихуана, связаны с нарушениями овуляции и снижением качества яйцеклеток.
• Осложнения беременности: употребление наркотиков во время зачатия или беременности может привести к выкидышу, врожденным дефектам и проблемам развития плода.
Отказ от употребления наркотиков имеет решающее значение для оптимизации фертильности и снижения рисков, связанных с беременностью.
Центр ЭКО на Северном Кипре
Центр ЭКО на Северном Кипре - это клиника по лечению бесплодия, ориентированная на пациентов, расположенная в «Элитный исследовательский и хирургический госпиталь» в Никосии, Кипр. Наша клиника является одной из самых передовых клиник по лечению бесплодия в мире, предлагающей более широкий выбор вариантов лечения по доступным ценам.
Главная
Телефон
Английский: +90 548 875 8000
Французский: +90 548 876 8000
Турецкий: +90 542 869 8000
Арабский: +90 548 875 8000
Немецкий: +90 548 830 1987
Русский: +90 548 828 9955
Электронная почта
info@northcyprusivf.net
© 2020 LowCostIVF - Все права защищены. политика конфиденциальности

