- معلومات عنا
- مدونة
- العقم
- علاجات أطفال الأنابيب
- التطورات الجديدة في عمليات التلقيح الصناعي
- علاج أطفال الأنابيب في قبرص
- أطفال الأنابيب للنساء فوق سن الأربعين
- التلقيح الصناعي للنساء فوق سن الخمسين
- IUI
- التلقيح الاصطناعي المصغر
- أطفال الأنابيب + الحقن المجهري
- التلقيح الاصطناعي السيتوبلازمي
- دورة التلقيح الاصطناعي الترادفية
- التبرع بالبويضات
- التبرع بالجنين
- التبرع بالحيوانات المنوية
- الجنس - اختيار الجنس
- تأجير الأرحام الحملي
- تأجير الأرحام مثلي الجنس من نفس الجنس
- سحب الحيوانات المنوية جراحيًا
- التشخيص الجيني قبل الزرع PGD
- تجميد البويضات
- اختيار الجنس باستخدام بيض المتبرع
- الوقاية من مرض فقر الدم المنجلي
- التعليمات
- يسافر
- معلومات عنا
- مدونة
- العقم
- علاجات أطفال الأنابيب
- التطورات الجديدة في عمليات التلقيح الصناعي
- علاج أطفال الأنابيب في قبرص
- أطفال الأنابيب للنساء فوق سن الأربعين
- التلقيح الصناعي للنساء فوق سن الخمسين
- IUI
- التلقيح الاصطناعي المصغر
- أطفال الأنابيب + الحقن المجهري
- التلقيح الاصطناعي السيتوبلازمي
- دورة التلقيح الاصطناعي الترادفية
- التبرع بالبويضات
- التبرع بالجنين
- التبرع بالحيوانات المنوية
- الجنس - اختيار الجنس
- تأجير الأرحام الحملي
- تأجير الأرحام مثلي الجنس من نفس الجنس
- سحب الحيوانات المنوية جراحيًا
- التشخيص الجيني قبل الزرع PGD
- تجميد البويضات
- اختيار الجنس باستخدام بيض المتبرع
- الوقاية من مرض فقر الدم المنجلي
- التعليمات
- يسافر
أطفال الأنابيب للنساء فوق سن الأربعين
التلقيح الصناعي للنساء فوق سن الأربعين: مسارات واقعية ومُبشرة للمضي قدمًا
فهم المناظر الطبيعية:
مع تقدم النساء في السن، وخاصةً بعد سن الأربعين، نلاحظ انخفاضًا ملحوظًا في الخصوبة. ويعود ذلك أساسًا إلى أن النساء يولدن بعدد محدود من البصيلات، ويتناقص كلٌّ من الكمية والنوعية بمرور الوقت بسبب الإجهاد التأكسدي التراكمي، وخلل الميتوكوندريا، والأخطاء الانقسامية (تي فيلدي وبيرسون، ٢٠٠٢).
وفقًا لبيانات السجلّات الكبيرة، تنخفض معدلات الولادات الحية باستخدام بويضات غير متبرعة من حوالي 26% في سن 38-40 إلى حوالي 13% في سن 41-42، وإلى أقل من 5% بعد سن 42 (SART، 2023). يُظهر الرسم البياني أدناه تقديرًا تقريبيًا لاحتياطيات المبيض لدى المرأة المتوسطة طوال سنوات الإنجاب.
الشكل 1: العمر واحتياطي المبيض لدى الأنثى
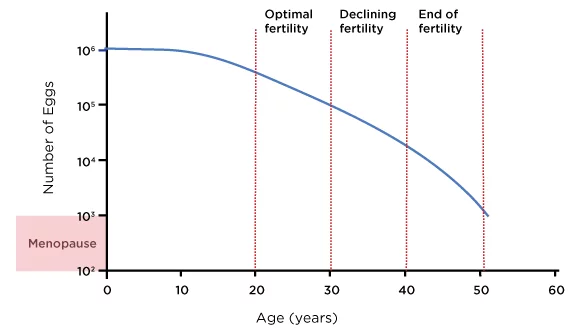
مصدر: أوزيجيت، أ. وأوزيجيت، س.، ٢٠١٨. دليل التلقيح الاصطناعي: ما تحتاج لمعرفته حول الخصوبة والعقم وخيارات العلاج المتاحة. الطبعة الأولى. إيرفين، كاليفورنيا: دار نشر يونيفرسال، الشكل ١.
مع ذلك، يختلف احتياطي المبيض واستجابته بين النساء، وتحافظ بعض النساء على قدرة إنجابية أعلى حتى أوائل الأربعينيات من العمر. هذا يجعل التقييم الشخصي عبر فحص عدد الجريبات الغارية (AFC) واختبار الهرمون المضاد لمولر (AMH) ونتائج دورة التلقيح الصناعي السابقة أمرًا أساسيًا لاختيار الاستراتيجية الأنسب (بروير وآخرون، ٢٠١٤).
بنك البويضات أو الأجنة: بناء "شبكة الأمان" الخاصة بك
أحد الأساليب العملية لتحسين معدلات النجاح التراكمي هو بنك البويضات أو الأجنة. فمن خلال الخضوع لدورات تحفيز واسترجاع متعددة، يُمكن تجميع عدد أكبر من البويضات (أو الأجنة)، مما يزيد من احتمالية نجاح الحمل. وقد ثبت أن تجميد البويضات يُحقق معدلات بقاء وإخصاب تُضاهي البويضات الطازجة (كوبو وآخرون، ٢٠١٦) دون زيادة خطر التشوهات الخلقية (نويس وآخرون، ٢٠٠٩). لذلك، يُمكن أن يُوفر استرجاع البويضات المتعددة أعدادًا لا يُمكن الحصول عليها باستخدام عملية استرجاع بويضة واحدة.
في حين أن معدلات الحمل والولادة الحية للنساء فوق سن الأربعين في دورة علاجية واحدة متواضعة نسبيًا، فمن المهم تذكر أن هذه الأرقام تُحسب لكل دورة علاجية. عند إجراء عدة دورات ودمج النتائج، يمكن أن يزداد احتمال الحمل والولادة الحية بشكل كبير. كما يوفر هذا النهج فرصة لإجراء اختبار جيني قبل الزرع للكشف عن اختلال الصيغة الصبغية (PGT-A)، والذي يمكن أن يساعد في تحديد الأجنة ذات المتممة الكروموسومية الطبيعية، ويزيد من فرص النجاح (دويل وآخرون، 2016).
يمكن أن يكون بنك البويضات أكثر فعاليةً عند دمجه مع التطورات الحديثة الأخرى في طب الإنجاب التي من شأنها تحسين نتائج الدورة الشهرية. من بين هذه التطورات: علاج البلازما الغنية بالصفائح الدموية للمبيض والابتكار التكنولوجي الحديث المعروف باسم العلاج باستبدال الميتوكوندريا (MRT). قد يُحسّن دمج هذه الأساليب مع بنوك البويضات جودة البويضات المُجمّعة وقدرتها التنموية، مما يزيد عدد الأجنة القابلة للحياة المتاحة للنقل. عند استخدامها بشكل استراتيجي، تُكمّل هذه الأساليب فوائد بنوك البويضات ليس فقط من خلال توسيع مجموعة البويضات المُخزّنة، بل أيضًا من خلال تحسين قدرتها الإنجابية، مما يُتيح في النهاية فرصة أكبر لتحقيق حمل ناجح.
بلازما المبيض الغنية بالصفائح الدموية (PRP)
يتضمن علاج الصفائح الدموية بالبلازما الغنية بالصفائح الدموية (PRP) في المبيض حقن مركز صفائح دموية ذاتية في المبيضين، بهدف تحفيز عوامل النمو الموضعية التي قد تعزز تجنيد الجريبات. وقد أفادت الدراسات التي أُجريت على النساء ذوات الاستجابة الضعيفة، بمن فيهن النساء في سن الإنجاب المتقدم، بتحسن في جودة هرمون AMH، وAFC، والكيسة الأريمية، مع تحقيق بعض الولادات الحية (Sfakianoudis وآخرون، 2019). وأظهرت دراسة حديثة زيادات ملحوظة في إنتاج الكيسة الأريمية القابلة للاستخدام بعد علاج الصفائح الدموية بالبلازما الغنية بالصفائح الدموية لدى النساء ذوات الأجنة ذات الجودة الرديئة سابقًا (Yu وآخرون، 2025). ورغم أن علاج الصفائح الدموية بالبلازما الغنية بالصفائح الدموية لا يزال غير معياري، إلا أنه يُعدّ مكملًا مناسبًا لمجموعة مختارة من المريضات الراغبات في تحسين إنتاج بويضاتهن.
يُعد علاج البلازما الغنية بالصفائح الدموية (PRP) للمبيض إجراءً أكثر تطورًا من مجرد حقن البلازما الغنية بالصفائح الدموية في المبايض على أمل التحسن. يعتمد نجاحه على بروتوكولات مُصممة بعناية تبدأ بالتحضير السليم للصفائح الدموية، بما في ذلك التثبيط المُتحكم به لمنع التنشيط المُبكر ونضوب عوامل النمو قبل الوصول إلى النسيج المُستهدف. يجب تحسين تركيز وكثافة الصفائح الدموية لضمان جرعة علاجية مُجدية، حيث قد تفشل المستحضرات غير المُثلى أو المُخففة بشكل مفرط في توفير المُحفز التجديدي المُراد. ومن الأمور بالغة الأهمية دقة الحقن مع استهداف مناطق تشريحية مُحددة داخل المبيض حيث يُرجح أن يستفيد نمو الجريبات من تعزيز الأوعية الدموية والإشارات الخلوية والدعم البيئي الدقيق. بعد الإجراء، يُعد اتباع نظام مُكملات مُخصص أمرًا ضروريًا للحفاظ على عملية تكوين البويضات ودعمها، مما يضمن أن تكون البيئة البيوكيميائية والهرمونية مُواتية لاستقطاب الجريبات ونموها ونضجها. تعمل هذه العوامل مجتمعة على تحويل علاج البلازما الغنية بالصفائح الدموية من مجرد حقنة بسيطة إلى تدخل علمي قائم على أساس علمي وربما يكون له تأثير تحويلي على وظيفة المبيض.
العلاج باستبدال الميتوكوندريا (MRT)
العلاج باستبدال الميتوكوندريا (MRT) هو تقنية إنجابية ناشئة تهدف إلى استعادة القدرة الحيوية للبويضات عن طريق تزويدها بميتوكوندريا سليمة من متبرعة. يعالج هذا النهج مباشرةً أحد أهم التغيرات المرتبطة بالعمر في الإنجاب لدى الإناث: التراجع التدريجي في وظيفة الميتوكوندريا، والذي ارتبط ارتباطًا وثيقًا بانخفاض كفاءة البويضة وضعف نمو الجنين (St. John et al., 2019).
من خلال إدخال الميتوكوندريا الوظيفية إلى البويضة، يهدف العلاج بالرنين المغناطيسي إلى تحسين إنتاج ATP، وتحسين البيئة الخلوية للانقسام الاختزالي، وتعزيز القدرة التنموية للأجنة الناتجة. على الرغم من حداثة تطبيقه السريري نسبيًا، إلا أن مركز شمال قبرص لأطفال الأنابيب يُعد من بين المرافق السريرية القليلة التي تقدم هذه الخدمة، وقد أظهرت الدراسات البشرية المبكرة وما قبل السريرية نتائج مشجعة، لا سيما لدى المرضى الذين يعانون من تاريخ من توقف نمو الأجنة المتكرر أو ضعف جودة الأجنة (تشانغ وآخرون، ٢٠١٧).
كان الدكتور شوخرات ميتاليبوف وزملاؤه في طليعة أبحاث نقل الميتوكوندريا، حيث أثبتوا في كل من النماذج الحيوانية والبويضات البشرية أن نقل الميتوكوندريا الصحية يمكن أن يصحح أوجه القصور في الطاقة الحيوية ويؤدي إلى تحسين نتائج الإخصاب وتطور الجنين، مما يدعم الأساس المنطقي لاستخدامه المستهدف في حالات قصور الميتوكوندريا المرتبط بالعمر أو المرض (كانج وآخرون، 2016).
استراتيجيات الجمع: بنك البويضات، وعلاج البلازما الغنية بالصفائح الدموية في المبيض، والتصوير بالرنين المغناطيسي
بالنسبة لبعض المريضات، وخاصةً اللواتي لديهن تاريخ من دورات فاشلة بسبب ضعف نمو الأجنة، قد توفر استراتيجية شاملة تجمع بين بنوك البويضات، وعلاج البلازما الغنية بالصفائح الدموية (PRP) في المبيض، وعلاج استبدال الميتوكوندريا، أفضل فرصة لتحسين النتائج. يستهدف هذا النهج متعدد الجوانب شيخوخة البويضات من عدة جوانب. يسمح بنوك البويضات بالحصول على بويضات فائضة، وهو ما لا يمكن تحقيقه باسترجاع بويضة واحدة في دورة التلقيح الصناعي. يهدف علاج البلازما الغنية بالصفائح الدموية في المبيض إلى تحسين البيئة الجريبية وتعزيز تجنيد الجريبات بشكل أكثر صحة من خلال دورة استرجاع البويضات، بينما يعمل علاج استبدال الميتوكوندريا على استعادة الطاقة الحيوية المثلى للبويضة وتحسين إمكانات نمو الجنين. تعالج هذه التدخلات معًا كلاً من إنتاج الطاقة الخلوية والبيئة الدقيقة للمبيض، وهما عاملان حاسمان في نجاح الإنجاب في حالات العقم المرتبط بالعمر (لابارتا وآخرون، 2019).
****
صُممت هذه الاستراتيجيات لتحسين فرص الحمل باستخدام المادة الوراثية للمرأة، مما يسمح بإنجاب طفل بيولوجي. مع أن هذه التدخلات قد تزيد بشكل كبير من فرص النجاح مقارنةً بدورة التلقيح الصناعي التقليدية، إلا أنها قد تنطوي على تكلفة مالية كبيرة ولا تضمن احتمالية نجاح عالية، خاصةً في حالات تقدم سن الأم أو انخفاض احتياطي المبيض. بالنسبة للأزواج أو الأفراد الذين لا يرغبون في التفكير في بويضات متبرعة، قد توفر هذه الأساليب تحسنًا ملموسًا في فرص إنجاب طفل بيولوجي. ومع ذلك، إذا كان الهدف الأساسي هو تحقيق الحمل وإنجاب طفل بغض النظر عن وجود صلة وراثية بالأم المقصودة، فإن الخيارات البديلة، مثل دورة التلقيح الصناعي المزدوج أو الاستخدام المباشر لبويضات متبرعة، يمكن أن توفر معدلات نجاح أعلى بكثير، خاصةً للنساء فوق سن الأربعين.
دورة التلقيح الاصطناعي الترادفية
دورة التلقيح الاصطناعي المزدوجة هو نهج علاجي تُحفّز فيه المريضة مبيضها لإنتاج بويضاتها الخاصة، مع استخدام بويضات متبرعة في الوقت نفسه خلال دورة العلاج نفسها. تُخصّب مجموعتا البويضات بشكل منفصل، وتُنتج أجنة من كل مصدر. يتيح هذا للوالدين المُراد إنجابهما محاولة الحمل باستخدام المادة الوراثية الخاصة بالمريضة، مع توافر أجنة متبرعة عالية الجودة في نفس الدورة. يمكن زراعة الأجنة من كلا المصدرين حتى مرحلة الكيسة الأريمية، واختبارها وراثيًا عند الرغبة، وحفظها للاستخدام مستقبلًا. يوفر هذا النهج ميزة فريدة تتمثل في تعظيم فرص نجاح العلاج خلال دورة علاجية واحدة مع الحفاظ على إمكانية وجود صلة بيولوجية بالأم المُراد إنجابها.
التبرع بالبويضات
التبرع بالبويضات يتضمن استخدام بويضات من متبرعة سليمة خضعت للفحص، تُخصب بحيوانات منوية من الأب المقصود أو بحيوانات منوية من متبرعة. ولأن جودة البويضات تعتمد بشكل كبير على عمر المتبرعة وصحتها الإنجابية، لا على الأم المقصودة، فإن هذا النهج يزيد بشكل كبير من احتمالية إنتاج أجنة عالية الجودة وتحقيق حمل ناجح. يُعدّ التلقيح الاصطناعي ببويضات متبرعة ذا قيمة خاصة للنساء في سن الإنجاب المتقدم، أو اللاتي يعانين من انخفاض حاد في احتياطي المبيض، أو اللاتي فشلت دورات التلقيح الاصطناعي السابقة ببويضاتهن. سيتشارك الطفل الناتج في صلة وراثية مع مصدر الحيوانات المنوية، ولكن ليس مع متلقية البويضة، مع بقاء تجربة الحمل والرابط بين الأم والجنين سليمين تمامًا.
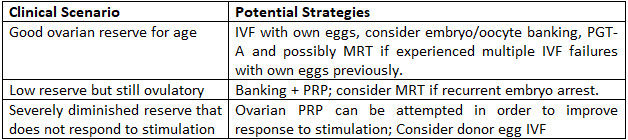
مسارات عملية للنساء فوق سن الأربعين
النقاط الرئيسية
- – إن النجاح في الحصول على بويضات بعد سن الأربعين أمر ممكن ولكنه يشكل تحديًا؛ والتوقعات الواقعية مهمة.
- - يمكن أن يؤدي بنك البويضات/الأجنة إلى تحسين الفرص التراكمية والسماح بالفحص الجيني.
- – MRT وPRP هي علاجات مضافة واعدة لحالات مختارة.
- - توفر البويضات المتبرعة أعلى معدلات النجاح ويجب مناقشتها في وقت مبكر إذا كان التشخيص سيئًا.
- لو سمحت اتصل بنا لمزيد من المعلومات والتوصيات المخصصة.
مراجع
- بروير، إس إل، وبروكمانز، إف جيه، ولافين، جيه إس، وفاوزر، بي سي، ٢٠١٤. الهرمون المضاد لمولر: اختبار احتياطي المبيض وتداعياته السريرية المحتملة. تحديث الإنجاب البشري، ٢٠(٥)، ص ٦٨٨-٧٠١.
- كوبو، أ.، غارسيا-فيلاسكو، ج.، كويلو، أ.، دومينغو، ج.، بيليسر، أ.، وريموهي، ج.، ٢٠١٦. تزجيج البويضات كخيار فعال للحفاظ على الخصوبة الاختيارية. مجلة الخصوبة والعقم، ١٠٥(٣)، ص ٧٥٥-٧٦٤.
- ديفروي، ب.، فوسر، ب. س.، وديدريش، ك.، ٢٠١١. مناهج لتحسين تشخيص العقم وإدارته. تحديث الإنجاب البشري، ١٧(٥)، ص ٤٥٥-٤٦٧.
- دويل، ج.و، ريختر، ك.س، ليم، ج.، ستيلمان، ر.ج، غراهام، ج.ر، وتوكر، م.ج، 2016. نجاح عملية تزجيج وتسخين البويضات الاختيارية والموصى بها طبيًا للتلقيح الصناعي الذاتي، مع توقع احتمالات الولادة للحفاظ على الخصوبة وفقًا لعدد البويضات المحفوظة بالتبريد وعمرها عند الاسترجاع. مجلة الخصوبة والعقم، 105(2)، ص. 459-466.
- Labarta، E.، de los Santos، MJ، Escribá، MJ، Pellicer، A. and Herraiz، S.، 2019. الميتوكوندريا كأداة لتجديد شباب البويضات. الخصوبة والعقم، 111(2)، الصفحات من 219 إلى 226.
- نويس، ن.، بوركو، إي.، وبوريني، أ.، ٢٠٠٩. أكثر من ٩٠٠ طفل حُفظت بويضاتهم بالتجميد وُلدوا دون زيادة واضحة في التشوهات الخلقية. مجلة الطب الحيوي التناسلي على الإنترنت، ١٨(٦)، ص ٧٦٩-٧٧٦.
- بولسون، آر جيه، هاتش، آي إي، لوبو، آر إيه، وساور، إم في، ٢٠٠٢. معدلات نجاح الحمل التراكمية بعد التبرع بالبويضات: الآثار المترتبة على قابلية بطانة الرحم للزرع. مجلة الإنجاب البشري، ١٧(٥)، ص ١٤١١-١٤١٦.
- ساور، إم في، 1990. تقرير أولي عن التبرع بالبويضات لتوسيع القدرة الإنجابية للنساء فوق سن الأربعين. مجلة نيو إنجلاند الطبية، 323(17)، ص 1157-1160.
- سفاكيانوديس، ك.، سيموبولو، م.، نيتسوس، ن.، وآخرون، ٢٠١٩. العلاج بالبلازما الغنية بالصفائح الدموية الذاتية يُمكّن امرأةً في سن اليأس المبكر من الحمل. تقارير حالات في صحة المرأة، ٢٣، e00129.
- سيلز، إي إس، ريكرز، إن إس، لي، إكس، وباليرمو، جي دي، ٢٠٢٠. أول بيانات عن التلقيح الصناعي بعد حقن بلازما غنية بالصفائح الدموية ذاتية المنشأ مُنشَّطة بغلوكونات الكالسيوم داخل المبيض. مجلة الغدد الصماء النسائية، ٣٦(٦)، ص ٤٧٩-٤٨٢.
- سانت جون، جيه سي، فاكوتشو-أوليفيرا، جيه، جيانغ، واي، كيلي، ر، وصلاح، ر، ٢٠١٩. نقل الحمض النووي للميتوكوندريا، وتضاعفه، ووراثته: رحلة من الأمشاج عبر الجنين إلى النسل والخلايا الجذعية الجنينية. تحديث التكاثر البشري، ٢٦(١)، ص ١-٣٥.
- يو، تي إن، وانغ، إتش واي، لي، تي إتش، وآخرون، ٢٠٢٥. حقن البلازما الغنية بالصفائح الدموية داخل المبيض يُحسّن بشكل ملحوظ إنتاج الكيسة الأريمية لدى مريضات التلقيح الصناعي اللواتي لديهن سابقًا ضعف في جودة الأجنة. التقارير العلمية، ١٥، ٨١٢٣٤.
- تشانغ، جيه، ليو، هـ، لو، س، وآخرون، ٢٠١٧. ولادة حية مشتقة من نقل مغزل البويضة للوقاية من أمراض الميتوكوندريا. مجلة الطب الحيوي التناسلي على الإنترنت، ٣٤(٤)، ص ٣٦١-٣٦٨.
مركز شمال قبرص لأطفال الأنابيب
مركز شمال قبرص لأطفال الأنابيب هو عيادة خصوبة تركز على المريض ، ويقع ضمن “مستشفى النخبة للأبحاث والجراحة"في نيقوسيا، قبرص. تعد عيادتنا واحدة من عيادات الخصوبة الأكثر تقدمًا في العالم، حيث تقدم مجموعة واسعة من خيارات العلاج بأسعار معقولة.
اتصل-بنا
هاتف
إنجليزي: +90 548 875 8000
فرنسي: +90 548 876 8000
اللغة التركية: +90 542 869 8000
عربي: +90 548 875 8000
ألمانية: +90 548 830 1987
الروسية: +90 548 828 9955
بريد إلكتروني
info@northcyprusivf.net
© 2020 LowCostIVF - جميع الحقوق محفوظة. سياسة الخصوصية


