- À propos
- Blog
- Infertilité
- Traitements de FIV
- Nouvelles avancées FIV
- Thérapie de remplacement mitochondrial!
- Traitement de FIV à Chypre
- IUI
- Mini FIV
- FIV + ICSI
- FIV cytoplasmique
- Cycle de FIV en tandem
- Don d'ovules
- Don d'embryons
- Don de sperme
- Genre – Sélection du sexe
- GPA gestationnelle
- Gestation pour autrui gay de même sexe
- Récupération chirurgicale de sperme
- Diagnostic Génétique Pré Implantation PGD
- Congélation d'oeufs
- Sélection du sexe à l'aide d'ovules de donneur
- Prévention de la drépanocytose
- FAQ
- Voyage
- À propos
- Blog
- Infertilité
- Traitements de FIV
- Nouvelles avancées FIV
- Thérapie de remplacement mitochondrial!
- Traitement de FIV à Chypre
- IUI
- Mini FIV
- FIV + ICSI
- FIV cytoplasmique
- Cycle de FIV en tandem
- Don d'ovules
- Don d'embryons
- Don de sperme
- Genre – Sélection du sexe
- GPA gestationnelle
- Gestation pour autrui gay de même sexe
- Récupération chirurgicale de sperme
- Diagnostic Génétique Pré Implantation PGD
- Congélation d'oeufs
- Sélection du sexe à l'aide d'ovules de donneur
- Prévention de la drépanocytose
- FAQ
- Voyage
Traitement Prp
Applications du plasma riche en plaquettes (PRP) pour la régénération cellulaire
Comment les thérapies PRP peuvent-elles aider à lutter contre l'infertilité féminine ?
La procréation assistée est un domaine scientifique dynamique qui évolue et se remodèle presque quotidiennement. La procréation assistée, dans sa définition simpliste, fait référence à l'obtention d'une grossesse avec l'aide de la science. L'aide de la science n'implique pas nécessairement l'utilisation d'équipements de haute technologie et de technologies extraterrestres ! Dans la plupart des cas, la procréation assistée est une simple reproduction des processus biologiques et physiologiques naturels du corps humain sur la base de nos connaissances et de notre compréhension actuelles. Grâce à la recherche et aux études cliniques, nous améliorons continuellement nos connaissances et notre conscience des processus biologiques et physiologiques naturels du corps humain, ce qui nous aide à concevoir de meilleurs schémas thérapeutiques pour nos patientes lors de leur préparation à la grossesse. En d'autres termes, plus nous comprenons comment notre corps fonctionne au niveau cellulaire, plus nous pouvons l'aider lorsqu'il a besoin d'un coup de main.
Plaquettes, également appelés thrombocytes, font partie de notre sang et participent à la cicatrisation des plaies et à la régénération des tissus. Le rôle des plaquettes est de reconnaître le site de la blessure (endothélium interrompu), d'adhérer au site de la blessure et de sécréter des messagers chimiques, activant ainsi le processus de cicatrisation. Le plasma riche en plaquettes (en abrégé PRP) est le produit sanguin où nous obtenons l'échantillon de sang d'un individu et utilisons des techniques de laboratoire pour séparer la partie du sang riche en plaquettes de la partie pauvre en plaquettes. Cela nous permet d'obtenir des concentrations élevées de plaquettes dans de petites quantités de plasma sanguin. Le but de l'obtention de plasma riche en plaquettes est d'amplifier et de multiplier ses effets curatifs naturels sur les tissus endommagés dans des périodes de temps relativement courtes lorsque les quantités naturelles ne suffisent pas à cette tâche.
Le PRP est une application thérapeutique régénérative relativement nouvelle et très prometteuse qui peut offrir plusieurs avantages thérapeutiques sans effets secondaires néfastes car il s'agit d'un produit direct de son propre échantillon de sang. Le PRP est très riche en plusieurs facteurs de croissance qui jouent un rôle important dans la régénération des tissus. Les principaux sont le facteur de croissance épidermique (EGF), le facteur de croissance endothélial vasculaire (VEGF), le facteur de croissance transformant bêta 1 (TGF-B1), le facteur de croissance transformant bêta 2 (TGF-B2), plusieurs classes de facteurs de croissance dérivés des plaquettes ( PDGF), le facteur de croissance analogue à l'insuline (IGF-1) et le facteur de croissance des hépatocytes (HGF). Ces facteurs de croissance fonctionnent de manière collective dans des parties clés de la régénération tissulaire telles que la croissance, la prolifération et la différenciation cellulaires en plus de l'amélioration de l'apport et de la circulation de l'oxygène. Alors que le PRP aide à la régénération des tissus via l'utilisation de facteurs de croissance, il a également la capacité de le faire sans provoquer de réponse inflammatoire grâce à ses molécules anti-inflammatoires telles que le facteur de croissance des hépatocytes.
Le PRP est actuellement utilisé à diverses fins, notamment des applications dermatologiques telles que l'anti-âge, la repousse des cheveux, les applications dentaires, ainsi que la régénération des tissus mous. Plus récemment, des essais cliniques et des tests sur des animaux ont fourni une quantité substantielle de preuves que le PRP peut avoir de nombreux effets bénéfiques dans le domaine de l'infertilité grâce à ses effets régénérateurs.
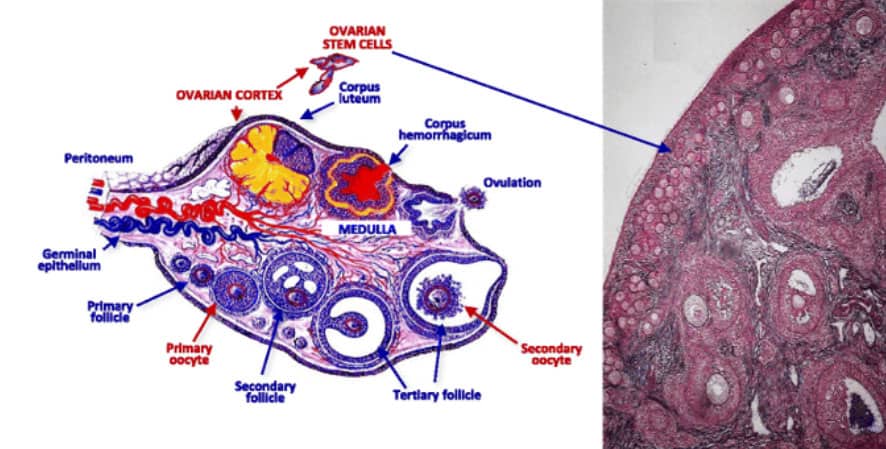
Application du PRP ovarien : rajeunissement ovarien
L'une des questions les plus fréquemment posées est de savoir si la ménopause peut ou non être inversée. Nos connaissances sur le sujet jusqu'à présent nous ont dit que non. Chaque femme naît avec un ensemble fini de réserves ovariennes et ces réserves diminuent avec le temps à chaque cycle menstruel. Cependant, les progrès récents de la recherche et des études cliniques indiquent que
possibilité de régénérer la fonction ovarienne même après la ménopause. Selon les dernières recherches menées par des scientifiques de Harvard, l'application de PRP dans le cortex ovarien peut éventuellement stimuler la lignée de cellules germinales à se développer en ovocytes ovariens. Les scientifiques ont réussi les tests sur les animaux et ont observé que l'injection de facteurs de croissance permettait la résurgence de la production d'ovocytes dans les ovaires.
Lorsque nous avons introduit ce traitement pour la première fois au centre de FIV de Chypre du Nord, il en était encore à un stade préliminaire de recherche. Au départ, les résultats obtenus étaient déroutants et pas à la hauteur de nos espérances. Cependant, en s'appuyant sur la recherche, le Dr Savas Ozyigit et son équipe ont remarqué que l'activation spontanée des plaquettes était un problème qui produisait peut-être des résultats mitigés chez les patients. D'autres modifications ont été apportées par les scientifiques de la FIV de Chypre du Nord au fil des ans et l'application du PRP ovarien n'est pas une modalité de traitement qui offre un succès considérable aux femmes dont la fonction ovarienne est diminuée ou épuisée.
D'après notre expérience jusqu'à présent, les femmes souffrant d'insuffisance ovarienne prématurée et de ménopause prématurée ont été le groupe qui a le plus bénéficié de cette option de traitement, ce qui suggère que l'âge reste une considération importante même lorsque les cellules souches sont impliquées.
Comment fonctionne l'application Ovarian PRP?
L'application de PRP dans les tissus mous ovariens vise la croissance et la prolifération cellulaires dans les ovaires sur la base de nombreuses propriétés des plaquettes. Les granules alpha sur les plaquettes se sont avérées riches en certains facteurs de croissance qui participent à la cicatrisation des plaies et à la régénération des tissus. Principal
ceux-ci incluent:
– Facteur de croissance épidermique (EGF),
– Facteur de croissance endothélial vasculaire (VEGF),
– Facteur de croissance transformant bêta 1 (TGF-B1),
– Facteur de croissance transformant bêta 2 (TGF-B2),
– Plusieurs classes de facteurs de croissance dérivés des plaquettes (PDGF), facteur de croissance analogue à l'insuline (IGF-1) et facteur de croissance des hépatocytes (HGF).
Le facteur de croissance épidermique (EGF) est un polypeptide unique de 53 résidus d'acides aminés qui est impliqué dans la régulation de la prolifération cellulaire.
Le facteur de croissance endothélial vasculaire (VEGF) est une protéine signal qui stimule la formation des vaisseaux sanguins.
Le TGF-β est un ensemble multifonctionnel de peptides qui contrôle la prolifération, la différenciation et d'autres fonctions dans de nombreux types de cellules.
Le PDGF est impliqué dans la croissance cellulaire, la division et la croissance des vaisseaux sanguins à partir de ses précurseurs.
Sur la base de l'activité connue et prévisible des facteurs de croissance endothéliale et vasculaire, une vascularisation accrue, un apport sanguin amélioré et une stimulation de la lignée de cellules germinales sont les avantages attendus d'une application PRP. Bien qu'il s'agisse d'un effet observé, on ne sait pas combien de temps la folliculogenèse peut être maintenue.
Il y a plusieurs considérations clés dans l'application du PRP ovarien si le succès doit être obtenu. Ces considérations importantes peuvent être grossièrement classées comme suit :
Méthode
L'isolement du PRP est l'un des principaux facteurs qui déterminent le succès des traitements PRP ovariens. Cela implique un certain nombre de considérations telles que :
– Anticoagulation de l'échantillon sanguin pour éviter l'activation prématurée des plaquettes
– protocoles de solation pour obtenir un échantillon hautement concentré
– Moment d'activation correct avant l'injection ovarienne
Emplacement
L'emplacement précis de l'injection de PRP est également un facteur clé de succès. Les cellules souches se trouvent uniquement dans le cortex ovarien. Par conséquent, tout traitement qui ne vise pas le cortex ovarien est voué à l'échec. Une injection de PRP d'une quantité très spécifique est injectée dans chaque cortex via un cathéter trans-vaginal, similaire à la procédure OPU. Le cathéter atteint l'extrémité du cortex et travaille vers l'arrière pour assurer une couverture corticale complète.
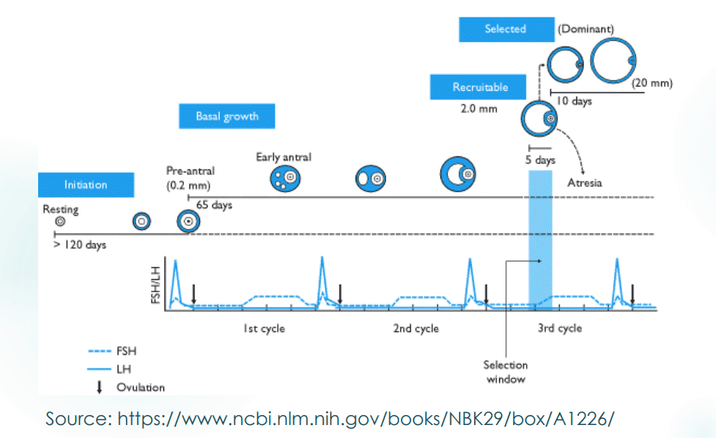
Oogenèse et moment du traitement
Tout traitement proposé aux couples pour la reproduction doit garder à l'esprit la physiologie de la reproduction. Toute action à entreprendre en matière de procréation assistée doit viser à imiter le plus possible la physiologie normale de la reproduction. Dans l'application du PRP ovarien, l'objectif est de restaurer la fonction ovarienne. En d'autres termes, nous visons à développer plus d'ovocytes en initiant l'ovogenèse sur la lignée des cellules souches dormantes. Connaître la chronologie de l'oogenèse nous indique exactement quelles mesures doivent être prises à différentes étapes pour soutenir le processus. Connaître le calendrier permet également de savoir quand les résultats souhaités doivent être attendus.
Vous trouverez ci-dessous un diagramme montrant différentes étapes de l'oogenèse dans une chronologie :
Traitements de soutien
- Hormone de croissance humaine
– Inhibiteurs de l'aromatase Il a été démontré qu'ils offrent un avantage supplémentaire dans le cadre du traitement PRP ovarien. Le moment précis de ces suppléments est également important lorsque l'on considère leurs avantages sur l'ovogenèse.
Sur la base de la chronologie d'une oogenèse réussie, nous nous attendons à ce que les lignées de cellules souches dormantes atteignent l'ovulation dans environ 4 mois. Cependant, les femmes en insuffisance ovarienne prématurée répondent dans des délais plus courts, en raison de l'existence de follicules primordiaux. Par conséquent, lors de la planification du traitement, le statut menstruel et l'âge de la patiente sont des considérations importantes.
Combien coûte l'application de PRP ovarien?
Y a-t-il des risques de rajeunissement ovarien avec le PRP ?
L'injection de PRP elle-même est pratiquement sans risque car le processus consiste à injecter dans les ovaires votre propre produit sanguin. Il n'y a pas de produits chimiques artificiels ou d'autres substances potentiellement nocives introduites dans votre corps. Cependant, le mode d'administration nécessite une sédation, tout comme vous seriez sous sédation dans un cycle de FIV pendant la collecte des ovules. Les effets secondaires de la procédure qui consiste à transférer vos plaquettes sanguines dans les ovaires sous sédation peuvent inclure une légère douleur après la procédure. Les effets secondaires très rares comprennent les saignements postopératoires et la fièvre.
Quels sont les avantages de l'application du PRP ovarien ?
Le principal avantage potentiel est la grossesse avec vos propres ovules même après la ménopause ! La réponse de chaque femme est différente et l'application du PRP peut ne pas fonctionner pour certaines femmes. Même lorsque cela fonctionne et que la ménopause est inversée, il faut garder à l'esprit que la ménopause est peut-être inversée pendant une période de temps relativement courte et cela peut ou non permettre une grossesse. Bien qu'il n'y ait aucune garantie, il s'agit de la dernière avancée en matière de technologies de reproduction qui peut potentiellement offrir une chance de grossesse avec les propres ovules d'une femme même lorsque ses réserves ovariennes sont épuisées. Les études préliminaires et les applications cliniques montrent de très bons résultats jusqu'à présent, donc compte tenu du coût relativement faible et des effets secondaires très minimes, une femme avec des réserves ovariennes épuisées qui aimerait avoir une chance de tomber enceinte avec ses propres ovules est très certainement une candidate idéale. .
Comment puis-je savoir que cela a fonctionné ?
Que sont les Exosomes ?
Les exosomes sont de minuscules nanovésicules présentes dans les espaces interstitiels ainsi que dans les fluides corporels. En raison de leur taille, les exosomes ont toujours été considérés comme des artefacts ou des déchets cellulaires sans fonction physiologique. Cependant, avec les progrès de la recherche dans le domaine de la médecine, ils sont maintenant connus pour faire partie d'un système de communication intracellulaire méticuleux.
Les exosomes sont connus pour leur implication dans tous les types de communication cellulaire. Ils fournissent des signaux autocrines locaux entre des types de cellules similaires, des signaux paracrines locaux entre différents types de cellules ainsi que des signaux endocriniens distants. Leur implication dans une signalisation cellulaire aussi étendue leur a valu le nom de « signalosomes ». Lorsque les exosomes sont introduits dans le corps, ils améliorent la communication via tous les canaux, ce qui contribue à la santé globale et à la fonction des cellules.
Par rapport aux cellules souches adultes, les exosomes contiennent 300% plus de facteurs de croissance, qui sont essentiels à la croissance, au développement et à la régénération cellulaires. Les exosomes peuvent être administrés par perfusion IV ou peuvent être dirigés vers un site spécifique par injection directe.
Demande de PRP endométrial
L'endométrite chronique et l'endométriose sont des problèmes qui peuvent déclencher des processus inflammatoires, ce qui peut rendre très difficile l'implantation d'embryons, soit par des rapports sexuels naturels, soit par fécondation in vitro (FIV). Lors de récents tests sur des animaux, il a été démontré que les applications de PRP ont des effets de prolifération cellulaire ainsi que des effets anti-inflammatoires tout en travaillant sur la réparation des tissus. L'application de PRP a également été associée à une activité accrue des récepteurs de la progestérone. Les récepteurs de la progestérone sont les principaux acteurs qui aident à maintenir une muqueuse endométriale épaisse et saine, qui à son tour, aide à l'implantation d'embryons.
Les études humaines offrent également des résultats identiques. Alors que les études en sont encore à leurs stades préliminaires, l'application commerciale a commencé en raison des avantages potentiels et de l'absence d'effets secondaires biologiques néfastes sur la base des études réalisées. Au centre de FIV de Chypre du Nord, nous avons maintenant commencé à proposer des applications PRP aux patientes atteintes d'endométrite chronique, aux patientes présentant des échecs d'implantation récurrents et de FIV ainsi qu'aux patientes qui ne peuvent pas obtenir le niveau souhaité d'épaisseur de l'endomètre pour un transfert d'embryon réussi.
Ci-dessous, vous pouvez voir la publication de recherche originale des scientifiques de Harvard qui ont jeté les bases de la régénération cellulaire ovarienne :
Nouvelles avancées dans les technologies de FIV
Centre de FIV de Chypre du Nord
Le centre de FIV de Chypre du Nord est une clinique de fertilité axée sur le patient, située dans "Hôpital de recherche et de chirurgie d'élite» à Nicosie, Chypre. Notre clinique est l’une des cliniques de fertilité les plus avancées au monde, offrant une plus large sélection d’options de traitement à des prix abordables.
Nous Contacter
Téléphone
Anglais: +90 548 875 8000
Français: +90 548 876 8000
Turc: +90 542 869 8000
Arabe: +90 548 875 8000
Allemand: +90 548 830 1987
Russe: +90 548 828 9955
info@northcyprusivf.net
© 2020 LowCostIVF - Tous droits réservés. politique de confidentialité

